Hydroxid vápenatý vzorec, vlastnosti, reaktivita a použitia
hydroxid vápenatý, tiež známe ako hydratované vápno alebo hasené vápno, je anorganická zlúčenina vzorca Ca (OH)2.
Hydroxid vápenatý má polymérnu štruktúru, podobne ako všetky hydroxidy kovov, identický s hydroxidom horečnatým (Mg (OH)).2) tiež známy ako brucita.
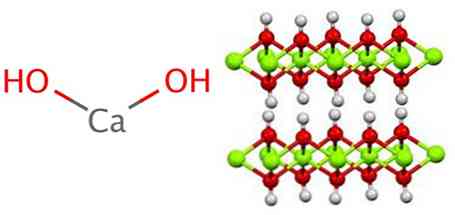
Je možné vidieť, že v tejto štruktúre vzniká vodíkové mosty. Hydroxid vápenatý sa syntetizuje priemyselne reakciou oxidu vápenatého, známeho aj ako vápno alebo pálené vápno, s vodou podľa nasledujúcej reakcie: \ t
CaOH + H2O → Ca (OH)2
Pripravuje sa tiež v laboratóriu reakciou medzi vodným chloridom vápenatým a hydroxidom sodným.
Hydroxid vápenatý sa vyskytuje prirodzene, ale zriedka vo svojej minerálnej forme ako portlandit, ktorý sa nachádza v niektorých sopečných a metamorfovaných horninách. (Hydroxid vápenatý vzorca - použitie hydroxidu vápenatého, vlastnosti, štruktúra a vzorec, 2005-2017).
Táto zlúčenina je tiež bežne dostupná v cementových, rozpúšťadlových a priemyselných čistiacich prostriedkoch (ako sú stavebné výrobky), odstraňovačoch podláh, čističoch tehál, cementových zahusťovacích produktoch a mnohých ďalších..
Vodný roztok sa bežne nazýva vápenná voda. Voda z vápna sa pripravuje miešaním hydroxidu vápenatého v čistej vode a filtráciou nadbytku Ca (OH).2 nerozpustené.
Keď sa do vápennej vody pridá nadbytok hydroxidu vápenatého, získa sa suspenzia častíc hydroxidu vápenatého, čím sa získa mliečny vzhľad, v takom prípade má bežný názov vápenného mlieka. Vápenné mlieko alebo nasýtený roztok vápna (vápenná voda) má pH 12,3 zásaditého charakteru.
Fyzikálne a chemické vlastnosti hydroxidu vápenatého
Hydroxid vápenatý je biely alebo bezfarebný prášok bez zápachu. Vo vodnom roztoku (nasýtené roztoky) má mliečny vzhľad vďaka supernatantu nerozpusteného hydroxidu vápenatého.
Nenasýtené roztoky sú zvyčajne číre a bezfarebné roztoky s miernym zemitým zápachom a horkou alkalickou chuťou hydroxidu vápenatého. Vzhľad zlúčeniny je znázornený na obrázku 3 (Royal Society of Chemistry, 2015)..

Hydroxid vápenatý má molekulovú hmotnosť 74,093 g / mol a hustotu 2,211 g / cm3 v tuhom stave. Má bod topenia 580 stupňov Celzia. Je slabo rozpustný vo vode, pričom je schopný rozpustiť 1,89 gramu na liter pri 0 ° C, 1,73 gramu na liter pri 20 ° C a 0,66 gramu na liter pri 100 ° C..
Je rozpustný v glycerole a v roztokoch kyselín. Je nerozpustný v alkohole (National Center for Biotechnology Information, S.F.).
Hydroxid vápenatý sa čiastočne rozpustí vo vode za vzniku roztoku nazývaného vápenná voda, čo je mierna báza. Voda z vápna alebo Ca (OH)2 (aq) Reaguje s kyselinami za vzniku solí a môže napadnúť niektoré kovy, ako napríklad hliník. Voda z vápna ľahko reaguje s oxidom uhličitým za vzniku uhličitanu vápenatého, čo je užitočný proces nazývaný karbonácia:
Ca (OH)2 + CO2 → CaCO3 + H2O
Nitroparafíny, nitrometán, nitropropán atď. Tvoria soli s anorganickými bázami, ako je hydroxid vápenatý. Tieto suché soli sú výbušné. Zlúčenina je chemicky podobná hydroxidu sodnému (NaOH) alebo oxidu sodnému (Na2O). Tieto neutralizujú kyseliny exotermicky za vzniku solí a vody.
Miešanie týchto materiálov s vodou môže spôsobiť nebezpečné množstvá tepla, pretože báza sa rozpúšťa alebo riedi. Bázy reagujú s určitými kovmi (ako je hliník a zinok) za vzniku oxidov alebo hydroxidov kovov a vytvárajú plynný vodík.
Bázy môžu iniciovať polymerizačné reakcie v polymerizovateľných organických zlúčeninách, najmä epoxidoch. Horľavé a / alebo toxické plyny sa môžu vytvárať s amónnymi soľami, nitridmi, halogénovanými organickými látkami, rôznymi kovmi, peroxidmi a hydroperoxidmi. Tento typ zlúčeniny často slúži ako katalyzátor (Chemical Datasheet CALCIUM HYDROXIDE, S.F.)..
Reaktivita a nebezpečenstvá

Hydroxid vápenatý je stabilná zlúčenina, hoci je nekompatibilná so silnými kyselinami. Je klasifikovaná ako dráždivá látka a medzi jej nebezpečenstvá môžeme vyzdvihnúť:
Je korozívna pre oči (spôsobujú poškodenie rohovky alebo slepotu) a pokožku (spôsobujú zápal a pľuzgiere).
Vdýchnutie prachu spôsobí podráždenie v gastrointestinálnom alebo respiračnom trakte, charakterizované pálením, kýchaním a kašľom. Ťažká nadmerná expozícia môže spôsobiť poškodenie pľúc, asfyxiu, bezvedomie alebo smrť. Zápal oka sa vyznačuje začervenaním, podráždením a svrbením (Karta bezpečnostných údajov materiálu, hydroxid vápenatý, 2013).
Opakovaná expozícia očí pri nízkej úrovni prachu môže spôsobiť podráždenie a lokálnu deštrukciu pokožky alebo dermatitídu na koži. Opakované vdychovanie prachu môže spôsobiť rôzny stupeň podráždenia dýchacích ciest alebo poškodenia pľúc.
Ak sa táto chemikália dostane do kontaktu s očami, okamžite ich umyte veľkým množstvom vody, občas zdvihnite dolné a horné viečka. Musí byť poskytnutá okamžitá lekárska pomoc. Pri práci s touto chemikáliou sa nesmú používať kontaktné šošovky.
Ak sa táto chemikália dostane do kontaktu s pokožkou, okamžite opláchnite pokožku kontaminovanú mydlom a vodou. Ak táto chemikália preniká do oblečenia, okamžite odstráňte odev a opláchnite pokožku vodou. Ak podráždenie pretrváva aj po umytí, vyhľadajte lekársku pomoc.
Ak sa vdýchne veľké množstvo tejto chemikálie, exponovaná osoba sa musí okamžite presunúť na čerstvý vzduch. Ak sa dýchanie zastavilo, vykonajte resuscitáciu z úst do úst a tiež udržujte obeť v teple av pokoji. Čo najskôr vyhľadajte lekársku pomoc.
Ak dôjde k požitiu, okamžite vyhľadajte lekársku pomoc a ak je to možné, ukážte nádobu alebo štítok (otrava hydroxidom vápenatým, 2017).
Manipulácia a skladovanie
- Zlúčenina by sa mala skladovať v suchom obale.
- Nepožívajte ani nevdychujte prach.
- Do tohto výrobku by sa nikdy nemala pridávať voda.
- V prípade nedostatočného vetrania prineste primerané dýchacie prístroje.
- Zabráňte kontaktu s pokožkou a očami.
- Uchovávajte mimo dosahu ako kyseliny.
- Uchovávajte nádobu tesne uzavretú.
- Uchovávajte nádobu na chladnom a dobre vetranom mieste. Neskladujte pri teplote nad 25 stupňov Celzia.
Použitie a aplikácie

Hydroxid vápenatý sa vyrába vo veľkom meradle, ľahko sa s ním manipuluje a vo všeobecnosti je lacný, preto existuje mnoho pozoruhodných použití a aplikácií..
Významnou aplikáciou hydroxidu vápenatého je ako flokulant pri čistení vody a odpadových vôd. Vytvára načechranú nabitú pevnú látku, ktorá pomáha pri odstraňovaní menších častíc z vody, čo vedie k ľahšiemu produktu.
Táto aplikácia je umožnená nízkymi nákladmi a nízkou toxicitou hydroxidu vápenatého. Používa sa aj pri úprave sladkej vody na zvýšenie pH vody. Účelom je, aby rúrky nekorodovali tam, kde je základná voda kyslá.
Ďalšia skvelá aplikácia je v papierenskom priemysle, kde sa používa pri výrobe hydroxidu sodného. Táto konverzia je zložkou známeho sulfátového procesu, ktorý sa používa pri extrakcii buničiny.
V systémoch na podporu života, ako je napríklad práčka s oxidom uhličitým, najmä v dýchacích respirátoroch s uzavretým okruhom, kde je hydroxid lítny, ktorý je viac žieravý, považovaný za príliš rizikový.
Používa sa ako prísada do bielenia a omietok, s tzv. Vápennými maltami. Pri výstavbe ciest slúži hydroxid vápenatý na zlepšenie kvality pôdy.
Podľa National Institutes of Health sa hydroxid vápenatý bežne používa v zubných prácach ako antimikrobiálna látka a je substanciou voľby na vytvorenie ochrannej vrstvy známej ako apikálna bariéra..
Apikálne bariéry sa bežne používajú ako prostriedok na zabránenie pulzovej nekróze v situáciách, keď by bola endodontická operácia obzvlášť ťažká, čo je zvyčajne výsledkom nezrelého trvalého zuba..
Keďže hydroxid vápenatý môže pomôcť dezinfikovať zub, ak už infekcia existuje, môže sa použiť ako krátkodobá liečba na zníženie bolesti a zápalu pri príprave na endodontickú operáciu (Gottfried Schmalz, 2009).
Slúži ako prísada do morskej vody, pretože redukuje CO2 v atmosfére a zmierňuje skleníkový efekt.
Pri výrobe kovov sa do prúdu odpadového plynu vstrekuje vápno, aby sa neutralizovali kyseliny, ako sú fluoridy a chloridy, pred ich uvoľnením do atmosféry..
Hydroxid vápenatý sa používa ako aktívna alkalická zložka v niektorých produktoch na relaxáciu vlasov.
Podľa Cornell Centra pre výskum materiálov, hydroxid vápenatý môže narovnať kučeravé vlasy, pretože rozbije disulfidové väzby, ktoré spájajú cysteíny, aminokyseliny, ktoré sú prítomné vo vyšších koncentráciách v prirodzene kučeravých vlasoch. Porušenie týchto väzieb a ich utesnenie hydroxidom vápenatým permanentne mení fyzickú štruktúru ošetrených vlasov.
V zmesi Bordeaux slúži hydroxid vápenatý na neutralizáciu roztoku a vytvorenie dlhodobo fungicídu.
Používa sa v rafinériách ropy na výrobu olejových prísad (salicylátov, sulfátov, fenolov), v petrochemickom priemysle na výrobu tuhých olejov rôznych značiek a tiež v chemickom priemysle na výrobu stearátu vápenatého. , Bežne sa používa na skúmanie absorpcie oxidu uhličitého a plynu.
Hydroxid vápenatý sa používa pri výrobe brzdových doštičiek, pri príprave suchých zmesí na maľovanie a zdobenie a tiež pri výrobe zmesí pesticídov..
Používa sa tiež ako doplnok vápnika a pH / uhličitanový pufor pre korálovú akvakultúru v útesových akváriách.
Je to "alternatívny" prírodný insekticíd, väčšina z plazenia hmyzu, zomiera kontaktom s ním vrátane kliešťov, blch, chrobákov a lariev (Russiver, 2015).
Hydroxid vápenatý je účinným riešením na oddeľovanie vlasov od usní zvierat pri ich príprave na výrobu kože.
Zmes hydroxidu vápenatého a teplej vody vytvára kúpeľ, v ktorom by mali byť čerstvé kože nasiaknuté až štyri dni a často sa trepať. Tento proces uvoľňuje vlasy a pokožku do takej miery, že sa môže zvyčajne odstrániť ručne.
Kvôli svojej nízkej toxicite a mäkkosti svojich základných vlastností sa hasené vápno široko používa v potravinárskom priemysle na:
- Objasniť surovú šťavu z cukrovej trstiny alebo cukrovej repy v cukrovarníckom priemysle, procesnú vodu pre alkoholické nápoje a nealkoholické nápoje, nakladanú zeleninu a iné potraviny.
- Make kukuričné tortilly (pomôcť kukuričná múka prísť spolu). Kukurica varená s limetkou je premenená na nixtamal, čo výrazne zvyšuje biologickú dostupnosť niacínu, je tiež považované za chutnejšie a ľahšie stráviteľné.
- Pri výrobe soli na potravinárske a farmaceutické účely vyčistite soľanku z uhličitanov vápenatých a horečnatých.
- Posilniť ovocné nápoje, ako je pomarančová šťava a dojčenská výživa (BAUM, 2013).
referencie
- BAUM, J. (2013, 16. august). Použitie hydroxidu vápenatého. Zdroj: livestrong.com: livestrong.com.
- Hydroxid vápenatý Vzorec - hydroxid vápenatý Použitie, vlastnosti, štruktúra a vzorec. (2005-2017). Zdroj: softschools.com.
- Otrava hydroxidom vápenatým. (2017, 7. február). Získané z medlineplus.gov.
- Chemický technický list CALCIUM HYDROXIDE. (S.F.). Zdroj: cameochemicals.noaa.gov.
- Gottfried Schmalz, D. A. (2009). Biokompatibilita dentálnych materiálov. Berlin: springer.
- Karta bezpečnostných údajov materiálu Hydroxid vápenatý. (2013, 21. máj). Získané z sciencelab: sciencelab.com.
- Národné centrum pre informácie o biotechnológiách. (S.F.). PubChem Compound Database; CID = 6093208. Zdroj: pubchem.ncbi.nlm.nih.gov.
- Kráľovská spoločnosť chémie. (2015). Hydroxid vápenatý. Zdroj: ChemSpider: chemspider.com.
- Russiver, M. (2015, 17. august). Na čo sa používa hydroxid vápenatý? Zdroj: quora: quora.com.


