Proteinázová charakteristika K, enzymatická aktivita a aplikácie
proteinázy K je enzým, ktorý patrí do skupiny serínových proteáz, tj, že má vo svojom strede katalyticky aktívneho serín aminokyselín a má funkciu lámanie peptidové väzby hydrolýzou. Na druhej strane, tento enzým patrí do rodiny proteínov subtilizínu (peptidázy S8).
Proteináza K má molekulovú hmotnosť (MW) 28,900 daltonov a bola izolovaná prvýkrát v roku 1974 z extraktov huby Engyodontium album, predtým známe pod názvom Tritirachium album Limber.
Predstavuje vysokú proteolytickú kapacitu, ktorá je schopná degradovať prítomný keratín vo vlasoch. Slovo keratín v angličtine je napísané "keratín", preto sa nazýva "proteináza K".
Kvôli svojej vysokej schopnosti štiepiť natívne proteíny je tento enzým užitočný v rôznych technikách molekulárnej biológie. Používa sa hlavne na izoláciu a prípravu nukleových kyselín s vysokou molekulovou hmotnosťou (MW)..
Proteináza K pôsobí na uvoľnenie jadrovej DNA, zatiaľ čo ničí proteíny a deaktivuje RNázy a DNázy, teda odstraňuje nukleázy v prípravkoch DNA a RNA.
Okrem toho sa zistilo, že proteináza K môže hydrolyzovať nejaký denaturovaný natívny proteín, ktorý vzbudil záujem výskumných pracovníkov pre použitie pri štúdiu priónových proteínov (PrPC).
Napriek svojej vysokej proteolytickej účinnosti však existujú proteíny, ktoré sú rezistentné voči pôsobeniu proteinázy K. Medzi nimi sú niektoré abnormálne proteíny nazývané prióny (PrPSc) spojené s prenosnými spongiformnými encefalopatiami.
index
- 1 Charakteristika proteinázy K
- 2 Enzymatická aktivita
- 3 Aplikácie
- 4 Výhody proteinázy K
- 5 Proteíny rezistentné na proteinázu K
- 6 Referencie
Charakteristika proteinázy K
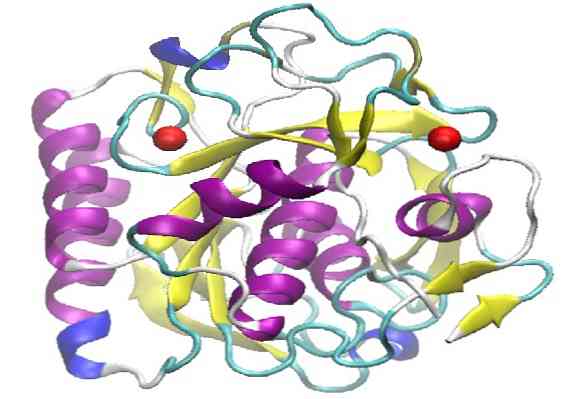
Proteináza K má terciárnu štruktúru skladajúci sa z troch vrstiev, s beta listu inmiscuidas siedmich reťazci medzi dvoma vrstvami špirál. Patrí do rodiny z peptidázy S8 je charakterizovaný jeho aktívne miesta v katalytickej triády, ktorého sekvenčné poradie je (Asp, His a Ser), ktorá ich odlišuje od ostatných rodín peptidázy.
Tento enzým zo skupiny serínových proteáz sa vyznačuje hydrolýzou peptidových väzieb v blízkosti karboxylovej skupiny alifatických a aromatických aminokyselín..
Na druhej strane je schopný pôsobiť v prítomnosti určitých korozívnych látok, ako sú dodecylsulfát sodný (SDS), Tris-HCL a EDTA, ktoré sa používajú na pomoc denaturácii proteínov, čo spôsobuje stratu ich prirodzenej štruktúry..
Toto je predbežný krok pri príprave proteínov pre elektroforetickú techniku. Rozsah pH, pri ktorom proteináza K pôsobí, je pomerne široký (2,0 až 12,0), s optimálnym pH medzi 7,5 až 12,0 a jeho izoelektrický bod je 8,9. Ako je možné pozorovať, je účinný proti veľmi širokému rozsahu pH.
Ďalšou charakteristikou, ktorá sa vyznačuje proteinázou K je jej stabilita v prítomnosti vysokých teplôt (50 - 60 ° C)..
Enzymatická aktivita
Proteináza K potrebuje prítomnosť vápnikového iónu, hoci to nemá vplyv na jeho aktivitu, ak je nevyhnutné zachovať jeho stabilitu.
Aby proteináza K vykonala úplné štiepenie substrátu, je potrebná približná doba kontaktu medzi 5 minútami a 2 hodinami..
Avšak v tejto súvislosti Daza kolies v porovnaní čistota DNA získaná niekoľkokrát expozície voči proteinázy K, a dospel k záveru, že predĺžená inkubácia (až 24 h), významne zlepšuje kvalitu DNA.
Teraz, vo vzťahu ku koncentrácii, ktorá sa používa v enzýme K enzýmu v rôznych protokoloch, možno povedať, že je veľmi rôznorodá.
Môže sa používať od veľmi nízkych koncentrácií (5 μg / ml) až po koncentrácie 500 μg / ml. Najčastejšie sa však pracovné koncentrácie pohybujú medzi 50-100 μg / ml, najmä pri trávení proteínov a inaktivácii nukleázy. Hoci je na ošetrenie tkaniva potrebná koncentrácia 2 mg / ml.
aplikácie
Jeho aplikácie sú veľmi široké a možno ich zhrnúť takto: \ t
-Používa sa pri štiepení proteínov a extrakcii DNA niekoľkými spôsobmi, ako sú: vysolenie, PK-SDS, cetyltrimetylamóniumbromid (CTAB), modifikovaný octan draselný a extrakcia jodidom sodným..
-Inaktivácia nukleáz (RNázy a DNázy).
-Pri hybridizačnej technike in situ (HIS), na uľahčenie uvoľňovania nukleovej kyseliny, okrem eliminácie nežiaducich proteínov.
-Modifikácia proteínu.
-Na úrovni výskumu, v rôznych štúdiách.
Výhody proteinázy K
Uskutočnilo sa niekoľko komparatívnych štúdií medzi DNA extrakčnými technikami s použitím Proteinázy K, pričom iné, ktoré ju nepoužívajú, a všetky dospeli k záveru, že pri použití enzýmu existujú väčšie výhody. Medzi výhodami možno spomenúť nasledovné:
-Získa sa DNA s vysokou molekulovou hmotnosťou vysokej kvality a čistoty.
-Extrahovaná DNA je stabilná až 3 mesiace.
Extrahovaná DNA sa môže použiť v nasledujúcich technikách: Southern blot, polymerázová reťazová reakcia (PCR), okrem iného elektroforéza..
Proteíny rezistentné na proteinázu K
Rôzne výskumy došli k záveru, že prióny (abnormálne PrPSc toxické proteíny) sa odlišujú od PrPC proteínov (natívnych), pretože sú rezistentné voči účinku proteinázy K, zatiaľ čo PrPC sú citlivé na ich účinok.
Ďalší autori opísali, že v štruktúre PrPSc existujú citlivé časti a iné rezistentné na proteinázu K. Avšak obe časti sú rovnako toxické a infekčné..
Na druhej strane, Bastian a spolupracovníci v roku 1987 izolovali 4 proteíny 28, 30, 66 a 76 kda z druhu Spiroplasma mirum. Všetky boli rezistentné voči účinku proteinázy K a tiež mali krížovú reakciu s niektorými priónmi.
Je známe, že tento druh môže spôsobiť šedý zákal a dôležité neurologické poškodenie a vďaka vedeckým zisteniam Bastiana sa medzi inými výskummi uskutočnil pokus o prepojenie tohto mikroorganizmu s prenosnými spongiformnými encefalopatiami..
Etiológia tejto degeneratívnej neurologickej patológie je však stále pripisovaná prionom.
V tomto zmysle Butler a spolupracovníci v roku 1991 identifikovali a charakterizovali triedu proteínov K rezistentných na 40 proteináz Kda z dvoch kmeňov Mycoplasma hyorhinis. Tento patogén postihuje ošípané, infikuje ich tkanivá, ale v tomto prípade nebola s testovanými priónmi žiadna krížová reakcia.
Na objasnenie mnohých neznámych je potrebný ďalší výskum.
referencie
- Bastian F, Jennings R., a Gardner W. 1987. Antisérum proti vláknitému proteínu asociovanému so scrapie krížovo reaguje s Spiroplasma mirum fibrilných proteínov. J. Clin. Microbiol. 25: 2430-2431.
- Daza C, Guillen J, King J, Ruiz V. Vyhodnotenie metódy extrakcie a purifikácie DNA zo svalového tkaniva fixovaného vo formaldehyde z neidentifikovaných mŕtvol. Med Magazine, 2014; 22 (1): 42-49,
- Butler G, Kotani H, Kong L, Frick M, Evancho S, Stanbridge E, a Mcgarrity G. Identifikácia a charakterizácia proteínov rezistentných na proteázu v členoch triedy Mollicutes. Infection and Immunity, 1991, 59 (3): 1037-1042
- López M, Rivera M, Viettri M, Lares M, Morocoima A, Herrera L a kol. Porovnanie dvoch protokolov na extrakciu DNA z Trypanosoma cruzi pestované v axenickom médiu. Peru. Med 2014; 31 (2): 222-227. K dispozícii na: scielo.org
- Jiménez G, Villalobos M, Jiménez E a Palma W. Stanovenie účinnosti piatich protokolov extrakcie DNA z parafínového materiálu na molekulárne štúdie. Rev Méd Univ Kostarika. 2007; 1 (1): 10-19.


