Vzorec na báze oxidu lítneho, vlastnosti, riziká a použitia
oxid lítny "Anorganická chemická zlúčenina vzorca Li" je anorganická chemická zlúčenina vzorca Li2Alebo sa tvorí spolu s malými množstvami peroxidu lítia, keď sa lítiový kov spaľuje vo vzduchu a kombinuje s kyslíkom.
Trh s kovmi a lítiom dominoval až do deväťdesiatych rokov americká výroba z ložísk nerastných surovín, ale na začiatku 21. storočia bola väčšina výroby odvodená z iných zdrojov než z USA; Najvýznamnejšími dodávateľmi na svete boli Austrália, Čile a Portugalsko. Bolívia má polovicu lítiových nánosov na svete, ale nie je veľkým producentom.
Najdôležitejšou komerčnou formou je uhličitan lítny, Li2CO3, vyrobené z minerálov alebo soľaniek niekoľkými rôznymi spôsobmi.
Keď sa lítium spaľuje vo vzduchu, hlavným produktom je biely oxid oxidu lítneho Li2O. Okrem toho sa vyrába nejaký peroxid lítia, Li2O2, tiež biela.
Môže sa tiež uskutočniť tepelným rozkladom hydroxidu lítneho, LiOH alebo peroxidu lítneho Li2O2.
4Li (s) + O2(g) → 2Li2O (s)
2LiOH + teplo → Li2O (s) + H2O (g)
2LI2O2(y) + teplo → 2Li2O (s) + O2(G)
Fyzikálne a chemické vlastnosti
Oxid lítny je biela tuhá látka známa ako lítia, ktorá nemá arómu a slanú chuť. Jeho vzhľad je znázornený na obrázku 2 (Národné centrum pre biotechnologické informácie, 2017).

Obrázok 2: vzhľad oxidu lítneho
Oxid lítny sú kryštály s antifloritovou geometriou podobnou geometrii chloridu sodného (kubický centrovaný na tvárach). Jeho kryštalická štruktúra je znázornená na obrázku 3 (Mark Winter [University of Sheffield and WebElements Ltd, 2016].
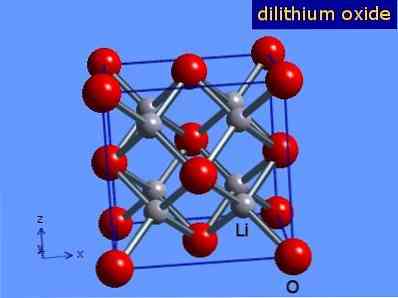
Obrázok 3: kryštalická štruktúra oxidu lítneho.
Jeho molekulová hmotnosť je 29,88 g / mol, jeho hustota je 2,013 g / ml a teploty topenia a varu sú 1438 ° C a 2066 ° C. Zlúčenina je veľmi rozpustná vo vode, alkohole, éteri, pyridíne a nitrobenzéne (Royal Society of Chemistry, 2015).
Oxid lítny ľahko reaguje s vodnou parou za vzniku hydroxidu a oxidu uhličitého za vzniku uhličitanu; preto sa musí skladovať a manipulovať s ním v čistej a suchej atmosfére.
Oxidové zlúčeniny nevedú k elektrickej energii. Niektoré štruktúrované oxidy perovskitu sú však elektronické vodivá, ktoré nachádzajú uplatnenie na katóde palivových článkov s pevným oxidom a systémov na výrobu kyslíka..
Sú to zlúčeniny, ktoré obsahujú aspoň jeden kyslíkový anión a jeden kovový katión (American Elements, S.F.)..
Reaktivita a nebezpečenstvá
Oxid lítny je stabilná zlúčenina nekompatibilná so silnými kyselinami, vodou a oxidom uhličitým. Podľa našich vedomostí neboli chemické, fyzikálne a toxikologické vlastnosti oxidu lítneho preskúmané a uvedené v hĺbke.
Toxicita zlúčenín lítia je funkciou ich rozpustnosti vo vode. Lítiový ión má toxicitu centrálneho nervového systému. Látka je silne žieravá, ak sa dostane do kontaktu s očami, pokožkou, pri vdýchnutí alebo požití (ESPI METALS, 1993).
V prípade kontaktu s očami by ste mali skontrolovať, či máte na sebe kontaktné šošovky a okamžite ich odstrániť. Oči by mali byť opláchnuté tečúcou vodou po dobu najmenej 15 minút, pričom viečka musia byť otvorené. Môžete použiť studenú vodu. Masti by sa nemali používať na oči.
Ak sa chemikália dostane do kontaktu s odevom, odstráňte ju čo najrýchlejšie, chráňte si vlastné ruky a telo. Položte obeť pod bezpečnostnú sprchu.
Ak sa chemikália akumuluje na exponovanej pokožke obete, napríklad na rukách, jemne a starostlivo umyte pokožku kontaminovanú tečúcou vodou a neabrazívnym mydlom. Môžete použiť studenú vodu. Ak podráždenie pretrváva, vyhľadajte lekársku pomoc. Kontaminovaný odev pred ďalším použitím vyperte.
V prípade vdýchnutia by mal byť obeť ponechaná na dobre vetranom mieste. Ak je inhalácia ťažká, obeť by mala byť čo najskôr evakuovaná do bezpečnej oblasti.
Uvoľnite tesné oblečenie, ako napríklad golier, remene alebo kravatu. Ak je pre obeť ťažké dýchať, musí sa podať kyslík. Ak obeť nedýcha, vykoná sa resuscitácia z úst do úst.
Vždy berte do úvahy, že môže byť nebezpečné pre osobu poskytujúcu pomoc pri ústach z úst do úst, keď je inhalovaný materiál toxický, infekčný alebo žieravý.
Vo všetkých prípadoch okamžite vyhľadajte lekársku pomoc (SIGMA-ALDRICH, 2010).
aplikácie
Oxid lítny sa používa ako tavidlo v keramických glazúrach a vytvára modrú s medom a ružami s kobaltom. Oxid lítny reaguje s vodou a parou, pričom vytvára hydroxid lítny a musí byť od nich izolovaný.
Oxid lítny (Li2O) s vysokým potenciálom trícia je atraktívnym kandidátom na pevnú kultúru materiálu DT fúznej elektrárne, vzhľadom na jeho vysokú hustotu atómov lítia (v porovnaní s inými lítiovými alebo kovovými lítiovými keramikami) a jej vodivosť relatívne vysoká tepelná (OXID LÍTI (Li2O), SF).
Li2Alebo bude vystavená vysokým teplotám pri ožarovaní neutrónov počas prevádzky fúznych prikrývok. Za týchto okolností sa v Li vyskytne veľký počet defektov ožiarenia2Alebo napríklad hélium indukované napučanie, relatívne vysoká tepelná rozťažnosť, rast zrna, tvorba LiOH (T) a zrážanie pri nízkych teplotách a transport hmoty LiOH (T) pri vysokých teplotách.
Okrem toho, Li2Alebo bude podliehať namáhaniu vyplývajúcemu z rozdielov v tepelnej rozťažnosti medzi Li2O a konštrukčné materiály. Tieto vlastnosti Li2Alebo vedú k náročným technickým problémom pri výrobe a dizajne deky.
Možné nové použitie je ako náhrada za kobalt a oxid lítny ako katóda v lítium-iónových batériách používaných na napájanie elektronických zariadení z mobilných telefónov na notebooky, ako aj na batérie poháňané batériami (Reade International Corp, 2016).
referencie
- Mark Winter [Univerzita v Sheffielde a WebElements Ltd. (2016). WebElements. Prevzaté z Lithium: dilithium oxid webelements.com.
- Americké prvky. (S.F.). Oxid lítny. Prevzaté z americanelements americanelements.com.
- ESPI METALS. (1993, jún). Oxid lítny. Prevzaté z espimetals espimetals.com.
- OXID LÍTI (Li2O). (S.F.). Prevzaté z ferp.ucsd.edu ferp.ucsd.edu.
- Národné centrum pre informácie o biotechnológiách. (2017, 24. jún). PubChem Compound Database; CID = 166630. Prevzaté z PubChem pubchem.ncbi.nlm.nih.gov.
- Reade International Corp. (2016). Prášok s oxidom lítnym (Li2O). Prevzaté z reade reade.com
- Kráľovská spoločnosť chémie. (2015). Oxid lítny.Prevzaté z chemspiderchemspider.com.
- Sigma-Aldrich. (2010). Karta bezpečnostných údajov materiálu Oxid lítny. Prevzaté z chemblink chemblink.com.


