Chemická štruktúra síranu amónneho, vlastnosti a použitie
síranu amónneho Je to ternárna a amoniakálna anorganická soľ kyseliny sírovej. Jeho chemický vzorec je (NH4)2SW4. Preto stechiometrické proporcie hovoria, že pre každý sulfátový anión sú s ním v interakcii dve amóniové katióny. To umožňuje neutralitu soli ((+1) ∙ 2 + (-2)).
Jeho názvoslovie je spôsobené tým, že ide o soľ odvodenú od H2SW4, zmena prípony "uric" na "ato". Dva počiatočné protóny sú teda nahradené NH4+, reakčný produkt s amoniakom (NH3). Potom chemická rovnica pre jeho syntézu je: 2 NH3 + H2SW4 => (NH4)2SW4
Síran amónny je sklad dusíka a síry, ktorý je nevyhnutný v chémii pôd a hnojív.
index
- 1 Chemická štruktúra
- 2 Fyzikálne a chemické vlastnosti
- 2.1 Molekulová hmotnosť
- 2.2 Fyzický vzhľad
- 2.3 Vôňa
- 2.4 Teplota topenia
- 2.5 Rozpustnosť
- 2.6 Hustota
- 2.7 Tlak pár
- 2.8 Bod vzplanutia
- 2,9 pH
- 2.10 Stabilita
- 2.11 Rozklad
- 2.12 Korózia
- 3 Použitie
- 3.1 V poľnohospodárstve
- 3.2 Ako analytické činidlo
- 3.3 Pri zrážaní a izolácii proteínov
- 3.4 V priemysle
- 3.5 Iné použitia
- 4 Odkazy
Chemická štruktúra
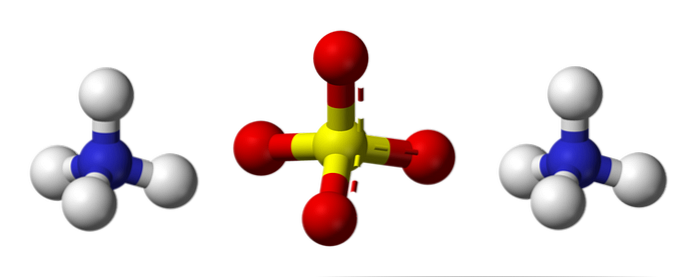
Horný obrázok znázorňuje molekulárnu geometriu iónov NH4+ a SO42-. Červené guľôčky zodpovedajú atómom kyslíka, biele guľôčky zodpovedajú atómom vodíka, modré guľôčky na atóme dusíka a žlté guľôčky zodpovedajú atómu síry..
Oba ióny sa môžu považovať za dva tetraedróny, ktoré majú tri jednotky, ktoré interagujú za vzniku ortorombického kryštálového usporiadania. Síranový anión je SO42- a je schopný darovať alebo prijímať štyri vodíkové väzby, podobne ako NH katión4+.
Fyzikálne a chemické vlastnosti
Molekulová hmotnosť
132,134 g / mol.
Fyzický vzhľad
Svieti biela. Ortorombické biele alebo hnedé kryštály, v závislosti od úrovne nečistôt.
vône
toaletný.
Teplota topenia
280 ° C. Táto teplota topenia, nízka v porovnaní s inými iónovými zlúčeninami, je spôsobená skutočnosťou, že ide o soľ s jednoväzbovými katiónmi (+1) a s rozdielnymi iónmi vo svojich veľkostiach, čo spôsobuje, že tuhá látka má nízko kryštalickú retikulárnu energiu.
rozpustnosť
76,4 g / 100 g vody pri 25 ° C. Táto afinita k vode je spôsobená veľkou kapacitou jej molekúl solvatovať amónne ióny. Na druhej strane je nerozpustný v acetóne av alkohole; v rozpúšťadlách menej polárnych ako voda.
hustota
1,77 g / cm3 pri 25 ° C.
Tlak pary
1,871 kPa pri 20 ° C.
Bod horľavosti
26 ° C.
pH
5,0 - 6,0 (25 ° C, 1 M roztok). Mierne kyslé pH je spôsobené hydrolýzou NH4+ vo vode, pričom vzniká H3O+ pri nízkych koncentráciách.
stabilita
Stabilný vo vhodných podmienkach prostredia. Pri kontakte so silnými oxidačnými činidlami sa môže vznietiť.
rozklad
Začína sa rozkladať pri 150 ° C, uvoľňuje toxické výpary oxidu siričitého, oxidov dusíka a amónia.
korózie
Nepoškodzuje železo ani hliník.
aplikácie

V poľnohospodárstve
- Síran amónny sa používa ako hnojivo v alkalických pôdach. Amónna soľ má vo svojom zložení 21% dusíka a 24% síry. Existujú však zlúčeniny, ktoré poskytujú väčšie množstvo dusíka ako síran amónny; Výhodou týchto látok je vysoká koncentrácia síry.
- Síra je nevyhnutná pri syntéze proteínov, pretože niekoľko aminokyselín - ako je cystín, metionín a cysteín - má síru. Z týchto dôvodov je síran amónny naďalej jedným z najdôležitejších hnojív.
- Používa sa v plodinách pšenice, kukurice, ryže, bavlny, zemiakov, konope a ovocných stromov.
- Nízke pH alkalických pôd v dôsledku ich príspevku k nitrifikačnému procesu vykonávanému mikróbmi. Použije sa amoniak (NH)4+) na výrobu dusičnanov (NO3-) a uvoľnenie H+: 2NH4+ + 4O2 => 2NO3- + 2H20 + 4H+. Zvýšenie koncentrácie vodíka znižuje pH alkalických pôd a umožňuje väčšie využitie.
- Okrem použitia ako hnojiva, síran amónny pôsobí ako pomocný prostriedok pre rozpustné insekticídy, herbicídy a fungicídy, ktoré sa rozprašujú na plodiny..
- Sulfát je schopný sekvestrovať ióny prítomné v pôde av zavlažovacej vode, ktoré sú nevyhnutné pre život určitých patogénov. Medzi iónmi, ktoré zachytáva síran amónny, patrí Ca2+, Mg2+, Viera2+ a viera3+. Toto pôsobenie zvyšuje mikrobicídny účinok uvedených činidiel.
Ako analytické činidlo
Síran amónny pôsobí ako zrážacie činidlo pri elektrochemickej analýze, v mikrobiologických kultivačných médiách a pri príprave amónnych solí..
Pri zrážaní a izolácii proteínov
Síran amónny sa používa pri izolácii a čistení proteínov, najmä plazmatických proteínov. Do plazmy sa pridá určité množstvo síranu amónneho do určitej koncentrácie; tak je spôsobená precipitácia skupiny proteínov.
Zrazenina sa oddelí odstredením a k supernatantu sa pridá ďalšie množstvo síranu amónneho a pri novej koncentrácii dôjde k vyzrážaniu inej skupiny proteínov..
Opakovanie predchádzajúceho postupu v sekvenčnej forme umožňuje získať rôzne frakcie plazmatických proteínov.
Predtým, ako sa objavia nové technológie molekulárnej biológie, tento postup umožnil izolovať plazmatické proteíny veľkého významu v medicíne, napríklad: imunoglobulíny, koagulačné faktory atď..
V priemysle
Síran amónny pôsobí na spomalenie začiatku požiaru v textilnom priemysle. Používa sa ako prísada v elektrolytickom priemysle. Používa sa tiež pri výrobe peroxidu vodíka, chloridu amónneho atď..
Iné použitia
- Síran amónny sa používa ako regulačné činidlo osmotického tlaku a ako činidlo zrážajúce soľ.
- Vo forme laurylsulfátu amónneho sa povrchové napätie vody znižuje, čo umožňuje separáciu znečisťujúcich látok zvýšením tvrdosti vody..
- Je to antikorózny prostriedok.
- Používa sa ako potravinárska prísada, ktorá reguluje kyslosť cesta v múke a chlebe.
referencie
- OECD SIDS. (Október 2004). Síran amónny. [PDF]. Získané 27. apríla 2018, z: inchem.org
- Spoločnosť Mosaic. (2018). Síran amónny. Získané dňa 27. apríla 2018, z: cropnutrition.com
- Wikipedia. (2018). Síran amónny. Získané dňa 27. apríla 2018, z: en.wikipedia.org
- PubChem. (2018). Síran amónny. Zdroj: 27. apríl 2018, z: pubchem.ncbi.nlm.nih.gov UpSticksNGo Crew.
- (23. júla 2015). [Obrázok]. Získané dňa 27. apríla 2018, z: flickr.com
- Paula Papp (22. február 2017). Aplikácia a použitie síranu amónneho. Získané dňa 27. apríla 2018, z: business.com


