Štruktúra, použitie, typy a toxicita síranu hlinitého (Al2 (SO4) 3)
síran hlinitý "Anorganická soľ hliníka vzorca Al."2(SO4)3, zvyčajne sa javí ako biela pevná látka s lesklými kryštálmi. Farba zlúčeniny bude ovplyvnená jej koncentráciou železa a akejkoľvek inej nečistoty. Existujú dva hlavné typy síranu hlinitého: A a B.
Na spodnom obrázku sú znázornené biele kryštály hydratovaného síranu hlinitého. Je možné pozorovať neprítomnosť hnedých sfarbení, čo svedčí o iónoch železa v kryštalickej mriežke.

Síran hlinitý je soľ, ktorá je veľmi rozpustná vo vode av prírode je zriedkavá nájsť ju v jej bezvodej forme. Zvyčajne sa hydratuje vo forme oktadekarátového síranu hlinitého [Al2(SO4)3.18H2O] alebo hexadekahydrát [Al2(SO4)3.16H2O].
Podobne môže tvoriť dvojité soli s draslíkom a s amónnymi zlúčeninami známymi ako hlinky. Čiastočne to môže byť spôsobené afinitou vody v hydrátoch na zadržanie iných iónov okrem hliníka.
Síran hlinitý sa môže rozkladať pôsobením vody v hydroxidu hlinitom a kyseline sírovej. Táto nehnuteľnosť umožnila jeho použitie ako okysľujúce pôdy.
Je to tiež toxická zlúčenina, najmä kontaktom s jej práškom. Má však nekonečné množstvo použití a aplikácií, ktoré idú od čistenia vody pomocou metódy koagulácie, ktorá sa deje prostredníctvom jej použitia v niekoľkých priemyselných odvetviach, až do jej použitia s terapeutickými cieľmi..
index
- 1 Štruktúra
- 2 Čo je to pre (použitie)
- 2.1 Koagulácia alebo flokulácia vody
- 2.2 Použitie ako moridlo atramentov a pri spracovaní papiera
- 2.3 Priemyselné použitie
- 2.4 Liečebné a terapeutické použitie
- 2.5 Iné použitia
- 3 Výroba síranu hlinitého
- 4 Typy
- 5 Toxicita
- 6 Referencie
štruktúra
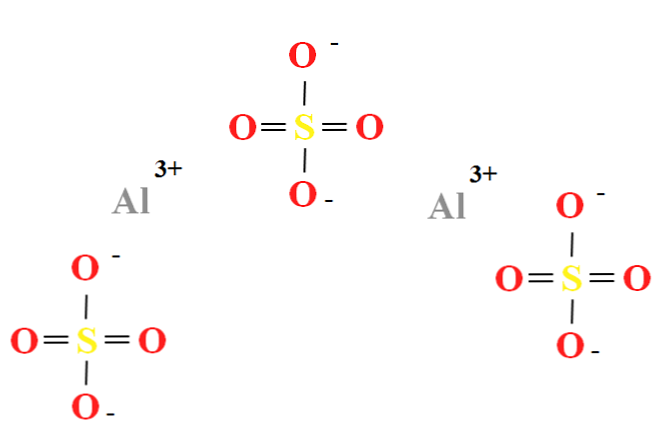
Síran hlinitý má pomer dvoch katiónov Al3+ za každé tri anionty SO42- (vrchný obrázok), ktorý možno pozorovať priamo v jeho chemickom vzorci Al2(SO4)3.
Všimnite si, že Al3+ sú sivasté, zatiaľ čo SO42- sú žlté (pre atóm síry) a červené (pre atómy kyslíka).
Zobrazená štruktúra zodpovedá bezvodej forme Al2(SO4)3, pretože žiadna molekula vody interaguje s iónmi. Vo svojich hydrátoch sa však voda môže priťahovať k pozitívnym centrám Al3+, alebo negatívnym SO tetraedrom42- cez vodíkové väzby (HOH-O-SO32-).
Al2(SO4)3∙ 18H2Alebo napríklad obsahuje 18 molekúl vody v pevnej štruktúre. Niektoré z nich môžu byť v priamom kontakte s Al3+ alebo SO42-. Inými slovami: síran hlinitý môže mať vnútornú alebo vonkajšiu koordinačnú vodu.
Jeho štruktúra môže tiež obsahovať iné katióny, ako je Fe3+, na+, K+, atď. Ale na to je potrebné prítomnosť viac aniónov SO42-. Za čo? Na neutralizáciu zvýšenia kladných poplatkov spôsobených kovovými nečistotami.
Síran hlinitý môže mať mnoho štruktúr, hoci jeho hydráty majú sklon prijať monoklinický kryštalický systém.
Fyzikálne a chemické vlastnosti
vzhľad
Vyzerá ako pevná látka s lesklými bielymi kryštálmi, granulami alebo práškom.
Molekulová hmotnosť
342,31 g / mol (bezvodý).
vône
Je bez zápachu
príchuť
Sladká chuť mierne sťahujúca.
Teplota topenia
770 ° C bezvodá forma (86,5 ° C oktadekadidátová forma)
Rozpustnosť vo vode
31,2 g / 100 ml pri 0 ° C; 36,4 g / 100 ml pri 20 ° C a 89 g / 100 ml pri 100 ° C.
hustota
2,67 až 2,71 g / cm3.
rozpustnosť
Mierne rozpustný v etylalkohole.
Tlak pary
V podstate nula.
stabilita
Stabilný vo vzduchu.
rozklad
Pri zahrievaní na približne teplotu topenia sa môže rozkladať najmä oxidom síry, toxickým plynom.
leptanie
Roztoky síranu hlinitého sú korozívne pre hliník. Tiež zlúčenina môže korodovať kovy v prítomnosti vlhkosti.
pKa
3.3 až 3.6. Jeho pH je 2,9 alebo viac v 5% vodnom roztoku.
Čo je to pre (použitie)
Koagulácia alebo flokulácia vody
-Keď sa zmieša s vodou (pitná, podávaná alebo odpad), síran hlinitý spôsobuje hydroxid hlinitý, ktorý tvorí komplexy so zlúčeninami a časticami v roztoku, ktoré urýchľujú ich sedimentáciu, čo by v neprítomnosti úpravy sulfátom hlinitým trvalo. dlho.
-Síran hlinitý sa používa aj pri čistení vody v bazéne, čo ich robí atraktívnejším na použitie.
-Použitím síranu hlinitého sa získava voda bez zakalenia a farby, čím sa zvyšuje jeho schopnosť uľahčovať čistenie vody. Tento spôsob čistenia však môže viesť k mierne zvýšenej koncentrácii hliníka vo vode.
-Hliník je veľmi toxický kov, ktorý sa hromadí v koži, mozgu a pľúcach a spôsobuje vážne poruchy. Okrem toho nie je známe, akú funkciu plní v živých bytostiach.
-Európska únia vyžaduje, aby maximálny povolený limit hliníka vo vode nepresiahol 0,2 mg / l. Agentúra Spojených národov na ochranu životného prostredia požaduje, aby maximálny limit kontaminácie vody s hliníkom nepresiahol 0,05 - 0,2 mg / l..
-Spracovanie odpadovej vody alebo použitie síranu hlinitého umožňuje ekonomicky eliminovať alebo redukovať fosfor v nich.
Použitie ako moridlo atramentov a pri spracovaní papiera
-Síran hlinitý sa používa ako moridlo pre farbivá alebo atramenty, čo pomáha fixovať materiál, ktorý sa má farbiť. Jeho fixačný účinok je spôsobený Al (OH)3, ktorých želatínová konzistencia prispieva k adsorpcii farbív na textíliách.
-Aj keď sa používa už od roku 2000 pred Kristom na opísaný účel, iba organické farbivá vyžadujú moridlá. Syntetické farbivá na druhej strane nevyžadujú moridlá, aby plnili svoju funkciu.
-Vytesnila sa z výroby papiera, ale stále sa používa pri výrobe papieroviny. Odstraňuje nečistoty, rovnako ako sa používa na viazanie materiálov, neutralizuje náboje a kalibruje kolofóniu.
Priemyselné použitie
-Používa sa v stavebníctve, aby urýchlil tuhnutie betónu. Okrem toho sa používa pri hydroizolácii budov.
-V priemysle mydiel a tukov sa používa na výrobu glycerínu.
-Používa sa v ropnom priemysle pri výrobe syntetických katalyzátorov, ktoré sa používajú počas prevádzky.
-Používa sa vo farmaceutickom priemysle ako adstringent pri príprave liekov a kozmetiky.
-Zasahuje do výroby farbív, ako je karmín. Používa sa tiež ako farbivo pri výrobe syntetických kaučukov butadiénového styrénu.
-V priemysle výroby cukru sa používa ako čistička melasy pre cukrovú trstinu.
-Používa sa pri výrobe deodorantov. Prečo? Pretože spôsobuje zúženie kanálikov potných žliaz, čím sa obmedzuje hromadenie potu, je to nevyhnutné médium pre rast baktérií, ktoré spôsobujú zápach..
-Používa sa pri opaľovaní kože, čo je nevyhnutný proces na jej použitie. Okrem toho sa používa pri výrobe hnojív.
-Používa sa ako prísada pri príprave náterových hmôt, lepidiel a tesniacich materiálov, ako aj čistiacich a ošetrovacích prostriedkov na nábytok..
Liečebné a terapeutické použitie
-Síran hlinitý je imunologické adjuvans. Preto plní funkciu spracovania antigénov takým spôsobom, že keď sa uvoľnia na svojom mieste pôsobenia, produkujú väčšiu produkciu protilátok pre antigény, ktoré boli inokulované..
-Freundovo adjuvans a BCG, ako aj iné adjuvanty, vrátane endogénnych, ako sú interleukíny, sú nešpecifické pre antigény, čo umožňuje zvýšenie polomeru imunitného pôsobenia. To umožnilo vývoj vakcín proti mnohým chorobám.
-Koagulačný účinok síranu hlinitého umožnil elimináciu mnohých vírusov v upravenej vode, okrem iného: Q beta, MS2, T4 a P1. Výsledky ukazujú, že spracovanie vody pomocou síranu hlinitého spôsobuje inaktiváciu takýchto vírusov.
-Síran hlinitý sa používa vo forme tyčinky alebo ako prášok na ošetrenie malých povrchových rán alebo odrenín vznikajúcich pri holení..
-Používa sa pri výrobe octanu hlinitého, zlúčeniny používanej pri liečbe niektorých stavov ucha. To bolo tiež použité, bez významného úspechu, na zmiernenie následkov požiaru uhryznutie..
-Roztoky síranu hlinitého sa používajú v koncentrácii 5% až 10% pri lokálnej liečbe vredov, ktoré umožňujú kontrolu ich sekrétov..
-Prísny účinok síranu hlinitého uzatvára povrchové vrstvy kože, koaguluje proteíny a hojí rany..
Iné použitia
-Síran hlinitý pomáha pri regulácii nadmerného rastu rias v rybníkoch, jazerách a vodných tokoch. Používa sa aj pri odstraňovaní mäkkýšov, okrem iného španielskeho slimáka.
-Záhradníci aplikujú túto zlúčeninu na okyslenie alkalických pôd. Pri kontakte s vodou sa síran hlinitý rozkladá na hydroxid hlinitý a zriedená kyselina sírová. Potom sa vyzráža hydroxid hlinitý, pričom sa kyselina sírová ponechá v roztoku.
-Okysľovanie pôd spôsobených kyselinou sírovou je vizualizované veľmi kreatívnym spôsobom v dôsledku existencie rastliny nazývanej Hydrangea, ktorej kvety sa modlia v prítomnosti kyslej pôdy; to znamená, že sú citlivé a reagujú na zmeny pH.
-Síran hlinitý sa podieľa na výrobe peny na boj proti požiaru. Ako? Reaguje s hydrogenuhličitanom sodným, čím sa uvoľňuje CO2. Tento plyn blokuje prístup2 na miesto spaľovania materiálu; a následne aj prímerie, ktoré sa vyvíjalo.
Výroba síranu hlinitého
Síran hlinitý sa syntetizuje reakciou zlúčeniny bohatej na hliník, ako je bauxitová ruda, s kyselinou sírovou pri zvýšených teplotách. Nasledujúca chemická rovnica predstavuje reakciu:
na2O3 + H2SW4 -> Al2(SO4)3 + 3H2O
Síran hlinitý môže byť tiež vytvorený neutralizačnou reakciou medzi hydroxidom hlinitým a kyselinou sírovou podľa nasledujúcej reakcie: \ t
2 Al (OH)3 + 3H2SW4 + 12 H2O -> Al2(SO4)3.18H2O
Kyselina sírová reaguje s hliníkom za vzniku síranu amónneho a uvoľňovania molekúl vodíka vo forme plynu. Reakcia je schematizovaná nasledovne:
2 Al + 3H2SW4 -> Al2(SO4)3 + 3H2
typ
Síran hlinitý sa klasifikuje do dvoch typov: typ A a typ B. V prípade síranu hlinitého typu A sú tuhé látky biele a majú koncentráciu železa nižšiu ako 0,5%..
V prípade síranu hlinitého typu B sú tuhé látky hnedé a majú koncentráciu železa nižšiu ako 1,5%..
Existujú priemyselné odvetvia, ktoré vyrábajú síran hlinitý a majú rozdielne kritériá na ich klasifikáciu. Priemysel teda uvádza, že sa pripravuje síran hlinitý typu A s maximálnou koncentráciou 0,1% železa ako oxidu železitého. Zatiaľ čo pre typ B je maximálna koncentrácia železa 0,35%..
toxicity
-Síran hlinitý je zlúčenina, ktorá pôsobí toxicky pri kontakte s prachom, čím spôsobuje podráždenie kože av prípadoch, keď je kontakt častý, dermatitída.
-V očiach spôsobuje silné podráždenie, dokonca spôsobuje trvalé zranenia.
-Vdýchnutie spôsobuje podráždenie nosa a hrdla, čo môže spôsobiť kašeľ a vyrážky.
-Jeho príjem spôsobuje podráždenie žalúdka, nevoľnosť a vracanie.
-Existujú toxické účinky, ktoré, hoci nie sú priamo spôsobené sulfátom hlinitým, sú nepriamo spôsobené ich použitím. Toto je prípad určitých toxických účinkov hliníka, spôsobených použitím síranu hlinitého pri čistení vody.
-Pacienti, ktorí sú chronicky dialyzovaní s použitím solí pripravených v prečistenej vode, použitím síranu hlinitého, majú veľmi vážne zdravotné poruchy. Medzi týmito poruchami máme anémiu, demenciu dialýzou a zvýšenie počtu ochorení kostí.
referencie
- Wikipedia. (2018). Síran hlinitý Prevzaté z: en.wikipedia.org
- Aris Industrial Roztok síranu hlinitého typu A a B. Prevzatý z: aris.com.pe
- Christopher Boyd (9. júna 2014). Top Priemyselné použitie pre síran hlinitý. Prevzaté z: chemservice.com
- PubChem. (2018). Bezvodý síran hlinitý. Prevzaté z: pubchem.ncbi.nlm.nih.gov
- Andesia Chemicals (20. augusta 2009). Bezpečnostný list síranu hlinitého. [PDF]. Prevzaté z: andesia.com
- Chemická kniha. (2017). Síran hlinitý. Prevzaté z: chemicalbook.com


