Štruktúra, vlastnosti, použitie, chlorid sodný (NaCl)
chlorid sodný, tiež nazývaná bežná soľ alebo stolová soľ, je binárna anorganická soľ sodíka alkalického kovu a chlóru halogénu. Je to najväčšia zložka jedlej soli a jej minerálna forma je známa ako halit. Jej molekulárny vzorec je NaCl a opisuje stechiometrický pomer jeho iónov (Na+ cl-) a nie diskrétnej molekuly (Na-Cl)
Chlorid sodný je kryštalická biela pevná látka, ktorá je tvorená kombináciou sodíka, striebristého bieleho kovu, ktorý prudko reaguje s vodou a chlórovým prvkom, jedovatým, žieravým, bledozeleným plynom..

V hornom obrázku je znázornená časť kryštálov NaCl. Ako je možné, že dva prvky sú také nebezpečné ako Na a Cl2, môže sa vytvoriť jedlá soľ? Po prvé, chemická rovnica pre jej vytvorenie je:
2Na (s) + Cl2(g) => 2NaCl (s)
Odpoveď spočíva v povahe väzby v NaCl. Byť iónový, vlastnosti Na+ a Cl- sú diagonálne odlišné od tých neutrálnych atómov.
Sodík je životne dôležitým prvkom, ale vo svojej iónovej forme. Na+ je hlavný extracelulárny katión s koncentráciou približne 140 mEq / l a spolu s jeho sprievodnými aniónmi Cl- a HCO3- (hydrogenuhličitan), sú zodpovedné hlavne za hodnotu osmolarity a extracelulárneho objemu.
Okrem toho, Na+ Zodpovedá za tvorbu a vedenie nervových impulzov v neuronálnych axónoch, ako aj za iniciovanie svalovej kontrakcie.
NaCl sa používa už od staroveku na ochutenie jedla a na uchovanie mäsa, kvôli jeho schopnosti eliminovať baktérie a zabrániť znehodnoteniu.
Je tiež nevyhnutné na výrobu hydroxidu sodného (NaOH) a molekulárneho chlóru (Cl2) reakciou NaCl s vodou za hydrolýzy:
2H20 (l) + 2 NaCl (s) => 2NaOH (ac) + Cl2(g) + H2(G)
Na katóde (-) sa H akumuluje2 (g) a NaOH. Medzitým sa Cl akumuluje na anóde (+)2 (G). Hydroxid sodný sa používa pri výrobe mydiel a chlóru pri výrobe plastov z PVC.
index
- 1 Štruktúra chloridu sodného
- 1.1 Jednotná bunka
- 2 Vlastnosti
- 2.1 Molekulový vzorec
- 2.2 Molekulová hmotnosť
- 2.3 Fyzický popis
- 2.4 Farba
- 2.5 Chuť
- 2.6 Teplota varu
- 2.7 Teplota topenia
- 2.8 Rozpustnosť vo vode
- 2.9 Rozpustnosť v organických rozpúšťadlách
- 2.10 Hustota
- 2.11 Tlak pár
- 2.12 Stabilita
- 2.13 Rozklad
- 2.14 Viskozita
- 2.15 Korózia
- 2,16 pH
- 3 Použitie
- 3.1 V potravinách
- 3.2 Priemyselné použitie
- 3.3 Doma
- 3.4 Iné použitia
- 3.5 Terapeutické použitie
- 4 Toxicita
- 4.1 Požitie
- 4.2 Podráždenie a fyzický kontakt
- 5 Referencie
Štruktúra chloridu sodného
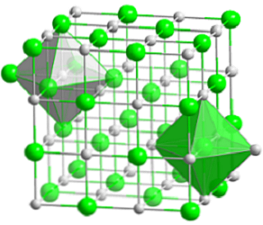
Kompaktná kubická štruktúra chloridu sodného je znázornená na hornom obrázku. Objemné zelené guľôčky zodpovedajú aniónom Cl-, biely, na katiónoch Na+. Všimnite si, že kryštál NaCl pozostáva zo siete iónov usporiadaných ich elektrostatickými interakciami v pomere 1: 1.
Hoci sú na obrázku znázornené stĺpce, väzby nie sú kovalentné, ale iónové. Použitie tyčiniek je užitočné pri znázornení koordinačnej geometrie okolo iónu. Napríklad v prípade NaCl každý Na+ je obklopený šiestimi Cl- (biely oktaedron) a každý Cl- šiestich Na+ (zelený oktaedron).
Preto má koordináciu (6,6), ktorej počet udáva, koľko susedov obklopuje každý ión. Číslo vpravo označuje susedov Na+, zatiaľ čo ten vľavo, Cl-.
Iné znázornenia vynechajú použitie tyčiniek na zvýraznenie oktaedrických otvorov, ktoré štruktúra má, čo vyplýva z intersticiálneho priestoru medzi šiestimi Cl aniónmi.- (alebo Na katióny+) balené. Toto usporiadanie je pozorované u iných mono (MX) alebo polyatomových anorganických solí a nazýva sa gemová soľ..
Jednotná bunka
Jednotková bunka kamennej soli je kubická, ale ktoré kocky presne reprezentujú na obrázku vyššie? Oktaedróny dávajú odpoveď. Obe pokrývajú celkom štyri malé kocky.
Tieto kocky majú časti iónov v ich vrcholoch, hranách a plochách. Pozorujúc pozorne, ión Na+ nachádza sa v strede a dvanásť z nich v okrajoch. Ión na jednom okraji môže byť zdieľaný štyrmi kockami. Takže existujú 4 Na ióny+ (12 × 1/4 + 1 = 4).
Pre ióny Cl-, osem je umiestnených vo vrcholoch a šesť na okrajoch. Keďže ióny umiestnené na vrcholoch zdieľajú priestor s ôsmimi ďalšími kockami a na okrajoch so šiestimi, majú 4 Cl ióny- (8 × 1/8 + 6 × 1/2 = 4).
Predchádzajúci výsledok sa interpretuje nasledovne: v jednotkovej bunke NaCl sú štyri katióny Na+ a štyri Cl anióny-; pomer, ktorý zodpovedá chemickému vzorcu (a Na+ pre každý Cl-).
vlastnosti
Molekulový vzorec
NaCl.
Molekulová hmotnosť
58,44 g / mol.
Fyzický popis
Kryštalická pevná látka.
farba
Priehľadné bezfarebné kryštály alebo biely kryštalický prášok.
príchuť
slaný.
Teplota varu
2,575 ºF až 760 mmHg.
1465 ° C.
Teplota topenia
1,474 ° F (800,7 ° C).
Ako bod varu, tak teplota topenia odrážajú teplo potrebné na prekonanie kryštalickej retikulárnej energie. Preto tieto merania potvrdzujú iónový charakter NaCl.
Rozpustnosť vo vode
Väčší alebo rovný 100 mg / ml pri 68 ° F.
36,0 g / 100 ml pri 25 ° C.
V skutočnosti je to hygroskopická soľ, ktorá zadržiava vlhkosť z prostredia.
Rozpustnosť v organických rozpúšťadlách
0,065 g / 100 ml etanolu pri 25 ° C; 10 g / 100 g glycerolu pri 25 ° C; 2,15 g / 100 ml kvapalného amoniaku pri 40 ° C; 1,4 g / 100 ml metanolu pri 25 ° C; 7,15 g / 100 etylénglykolu pri 25 ° C a 5,21 g / 100 g kyseliny mravčej pri 25 ° C.
hustota
2,165 g / cm3 pri 77 ° C.
Tlak pary
1 mmHg až 1 589 ° F.
stabilita
Je stabilný za odporúčaných skladovacích podmienok.
rozklad
Pri zahrievaní na vysoké teploty sa rozkladá výpary kyseliny chlorovodíkovej a oxidu disodného.
viskozita
Viskozita nasýtených roztokov 1,93 mPa-s.
korózie
Je korozívna pre mnoho kovov.
pH
6,7 až 7,3 vo vodnom roztoku.
aplikácie
V potravinách
-Chlorid sodný sa používa od staroveku na zlepšenie chuti potravín a ich ochrany. Solenie mäsa je spôsob, ako ho ochrániť pred bakteriálnym pôsobením, pretože oneskoruje rozklad bielkovín.
-Na druhej strane soľ zvyšuje osmolaritu okolo mäsa, čo spôsobuje absorpciu vody baktérií spôsobujúcich jej elimináciu osmózou..
Priemyselné použitie
Potravinársky priemysel
-V potravinárskom priemysle sa soľ používa ako zvýrazňovač chuti, prísada na kontrolu fermentácie, činidlo na kontrolu textúry a farbivo. Napríklad soľ sa pridáva na zvýraznenie farby slaniny, šunky a iných mäsových výrobkov.
-Soľ slúži ako spojivo pri výrobe klobás. Prispieva k tvorbe spojivového gélu zloženého z mäsa, tuku a vlhkosti.
-Pri spracovaní múky na výrobu chleba sa počas varenia pridáva soľ na kontrolu rýchlosti kvasenia cesta. Používa sa aj na posilnenie lepku a ako zvýrazňovač chuti, ako aj na plnenie pečiva.
-Používa sa pri výrobe raňajkových cereálií, zmiešaných alebo pripravených múčok, hranolkov, jedál pre psov a mačky atď..
Syntéza chemických výrobkov
-Chlorid sodný sa používa ako surovina pri výrobe hydroxidu sodného a chlóru, čo je zase užitočné v mnohých chemických odvetviach..
-Soľ sa používa pri spracovaní rôznych kovov, napríklad hliníka, medi, ocele a vanádu. Používa sa tiež na výrobu chlorečnanu sodného, ktorý sa následne používa pri syntéze oxidu chloričitého, bieliaceho prostriedku na báze kyslíka. Oxid chloričitý je menej škodlivý pre životné prostredie ako iné bielidlá.
V kožiarskom priemysle
-Soľ sa používa na inhibíciu bakteriálneho pôsobenia vo vnútri kože, ako aj na pomoc pri jej rehydratácii.
V textilnom priemysle
-Soľ sa používa ako moridlo pri farbení tkanín. Používa sa ako oplach solanky na odstránenie organických nečistôt a na vytvorenie pozitívneho náboja na povrchu tkanín, ktorý umožňuje spojenie záporne nabitých farbív..
V ropnom priemysle
-Pri prieskume ropy a zemného plynu je soľ dôležitou súčasťou vrtných vrtov. Používa sa na flokuláciu a zvýšenie hustoty vŕtacích kvapalín, čo umožňuje prekonať vysoké tlaky plynu v studniach, ktoré sa majú dosiahnuť. Okrem toho si soľ zachováva nasýtenie vŕtacej kvapaliny.
-Soľ pomáha zhutniť pôdu, na ktorej sú vybudované cesty. Znižuje posunutie spôsobené v podloží zmenami vlhkosti a automobilovej dopravy.
Doma
Soľ sa používa pri trení pri čistení povrchov, hrncov a panvíc. Tiež pri prevencii plesní a odstraňovač škvŕn. Tiež sa používa v mnohých značkách šampón a zubné pasty.
Iné použitia
Na cestách
-V očakávaní sneženia sú cesty pokryté soľankou, ktorá zabraňuje spojeniu ľadu s povrchom vozovky. Na rozmrazenie sa používa zmes soľanky a soli a niekedy sa pridávajú ďalšie chemické zložky, ako sú chloridy horečnaté alebo vápenaté. Použitie soli a soľanky nie je účinné pri teplotách pod -10 ° C.
Pri pridávaní soli dochádza k poklesu kryoskopického bodu, čo je koligatívna vlastnosť roztokov, čo nejakým spôsobom bráni tvorbe ľadu..
-V dôsledku svojho hygroskopického stavu sa soľ používa ako lacné sušidlo.
V živiciach používaných na zmäkčovanie vody
Tvrdá voda obsahuje ióny vápnika a horčíka, ktoré bránia pôsobeniu mydla a produkujú usadeniny alkalických materiálov v rôznych zariadeniach a potrubiach. Pri zmäkčovaní vody sa používajú ionomeničové živice. Soľ sa používa pri príprave a regenerácii živíc.
Na hasiacich prístrojoch
Chlorid sodný sa používa v hasiacich prístrojoch na hasenie požiarov, v ktorých sú prítomné horľavé kovy, ako sú zliatiny horčíka, draslíka, sodíka a NK..
Soľ pôsobí ako chladič a tiež ako drvič, ktorý obmedzuje prístup kyslíka k ohňu.
V okuliaroch
Kryštály chloridu sodného sa používajú v optických zložkách, ako sú okná a hranoly, najmä pre infračervené svetlo. Pretože je však soľ veľmi hygroskopická, vyskytuje sa určitý druh mrazu, ktorý pokrýva šošovky. Z tohto dôvodu boli šošovky chloridu sodného nahradené šošovkami so selenidom zinočnatým (ZnSe)..
Terapeutické použitie
Doplniť nedostatok solí v tele
-Keď je telo vyčerpanie Na+, musí byť nahradená, aby sa udržala extracelulárna osmolarita, nervová vodivosť a svalová kontrakcia.
-NaCl sa používa pri liečbe a prevencii nedostatku sodíka a chlóru, ktorý je dôsledkom nadmerného potenia počas vystavenia vysokým teplotám. Používa sa aj pri nadmernej diuréze alebo nadmernom obmedzení príjmu soli.
-Parenterálne podanie 045% roztoku NaCl sa používa na liečbu hyperosmolárneho diabetu. Spĺňa rehydratačnú funkciu a slúži na vyhodnotenie stavu funkcie obličiek.
-Injekcie hypertonických roztokov s koncentráciou NaCl vyššou ako 0,9% w / v,
-Používajú sa tam, kde dochádza k vážnej deplécii Na+, je obnovenie základného iónu. Táto hyponatrémia môže byť dôsledkom liečby voľnými elektrolytmi alebo koncentráciou Na+.
Hyponatrémia môže byť tiež spôsobená nadmerným príjmom vody, ktorý nie je kontrolovaný nedostatočnou renálnou funkciou.
V terapiách a netradičných použitiach
-Inhalačné roztoky NaCl sa používajú na riedenie liečiv používaných počas procesu nebulizácie. Používa sa aj na tracheálne umývanie a zavlažovanie. 0,9% fyziologický roztok používaný v nazálnych sprejoch.
-20% NaCl roztoky sa používajú na intra-amniotickú transabdominálnu inštaláciu, čím indukujú neskorý potrat počas druhého trimestra tehotenstva.
-Chlorid sodný sa môže použiť ako lokálne antiseptikum. Vďaka svojej osmotickej schopnosti je schopná dehydratovať široké spektrum vírusov a baktérií v nespálenom stave; preto sa používa ako bolestivé antiseptikum na dezinfekciu rán.
toxicity
požití
Má len škodlivý účinok na zdravie, ak je príjem vysoký a dlhý čas. Za týchto okolností by nastala hypernatrémia s následným zvýšením extracelulárneho objemu, čo by viedlo k vysokému krvnému tlaku.
Podráždenie a fyzický kontakt
Má toxický účinok len vtedy, ak je inhalácia veľmi vysoká. Pri kontakte s pokožkou v nadmernej forme môže spôsobiť jej suchosť. Nakoniec spôsobuje krátkodobé podráždenie pri kontakte s očami.
referencie
- Shiver & Atkins. (2008). Anorganická chémia (Štvrté vydanie, strany 84, 90, 93, 263). Mc Graw Hill.
- Whitten, Davis, Peck & Stanley. Chémia. (8. vydanie). CENGAGE Learning, str. 482-483.
- Chlorid sodný (2018). Chlorid sodný: Výhody, použitia, vlastnosti, riziká. Prevzaté z: clorurodesodio.org
- PubChem. (2018). Chlorid sodný. Zdroj: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2018). Chlorid sodný. Prevzaté z: en.wikipedia.org
- Americké prvky. (2018). Chlorid sodný. Prevzaté z: americanelements.com


