Vlastnosti jodičnanu draselného, štruktúra, použitie a riziká
jodičnan draselný alebo jodičnan draselný je anorganická zlúčenina jódu, konkrétne soľ, ktorej chemický vzorec je KIO3. Jód, prvok zo skupiny halogénov (F, Cl, Br, I, As), má v tejto soli oxidačné číslo +5; preto je to silné oxidačné činidlo. KIO3 disociuje vo vodnom médiu za vzniku K iónov+ a IO3-.
Je syntetizovaný reakciou hydroxidu draselného s kyselinou jódovou: HIO3(aq) + KOH (s) => KIO3(aq) + H2O (l) Tiež sa môže syntetizovať reakciou molekulového jódu s hydroxidom draselným: 3I2(s) + 6KOH (s) => KIO3(aq) + 5KI (aq) + 3H2O (l).

index
- 1 Fyzikálne a chemické vlastnosti
- 1.1 Oxidačné činidlo
- 2 Chemická štruktúra
- 3 Použitie a aplikácie jodičnanu draselného
- 3.1 Terapeutické použitie
- 3.2 Použitie v priemysle
- 3.3 Analytické použitie
- 3.4 Použitie v laserovej technológii
- 4 Zdravotné riziká jodičnanu draselného
- 5 Referencie
Fyzikálne a chemické vlastnosti
Je to biela tuhá látka bez zápachu, s jemnými kryštálmi a kryštalickou štruktúrou monoklinického typu. Má hustotu 3,98 g / ml, molekulovú hmotnosť 214 g / mol a má absorpčné pásy v infračervenom (IR) spektre.
Má bod topenia: 833 ºK (560 ºC), čo zodpovedá silným iónovým interakciám medzi iónmi K+ a IO3-. Pri vyšších teplotách podlieha tepelnému rozkladu, uvoľňujú molekulárny kyslík a jodid draselný:
2KIO3(s) => 2KI (s) + 3O2(G)
Vo vode má rozpustnosť, ktorá sa pohybuje od 4,74 g / 100 ml do 0 ° C, až do 32,3 g / 100 ml pri 100 ° C, čím sa vytvárajú bezfarebné vodné roztoky. Okrem toho je nerozpustný v alkohole a kyseline dusičnej, ale je rozpustný v zriedenej kyseline sírovej.
Jeho afinita k vode nie je citeľná, čo vysvetľuje, prečo nie je hygroskopická a neexistuje vo forme hydratovaných solí (KIO).3H2O).
Oxidačné činidlo
Jodičnan draselný, ako naznačuje chemický vzorec, má tri atómy kyslíka. Toto je silne elektronegatívny prvok a vďaka tejto vlastnosti "odhaľuje" elektronický nedostatok v oblaku obklopujúcom jód.
Tento nedostatok - prípadne príspevok - sa môže vypočítať ako oxidačné číslo jódu (± 1, +2, +3, +5, +7), ktoré je +5 pre prípad tejto soli..
Čo to znamená? Že pred druhom schopným dávať svoje elektróny, jód bude akceptovať ich vo svojej iónovej forme (IO)3-) na molekulárny jód a majú oxidačné číslo rovné 0.
Na základe tohto vysvetlenia je možné stanoviť, že jodičnan draselný je oxidačná zlúčenina, ktorá silne reaguje s redukčnými činidlami v mnohých redoxných reakciách; zo všetkých týchto je jeden známy ako jódové hodiny.
Jódové hodiny pozostávajú z redoxného procesu pomalých a rýchlych krokov, v ktorom sú rýchle kroky označené KIO riešením3 v kyseline sírovej, ku ktorej sa pridá škrob. Ďalej škrob - raz vyrobený a ukotvený medzi jeho štruktúrou druhu I3-- roztok zmení z bezfarebného na tmavomodrý.
IO3- + 3 HSO3- → I- + 3 HSO4-
IO3- + 5 I- + 6 H+ → 3 I2 + 3H2O
ja2 + HSO3- + H2O → 2 I- + HSO4- + 2 H+ (tmavo modrá v dôsledku škrobového efektu)
Chemická štruktúra
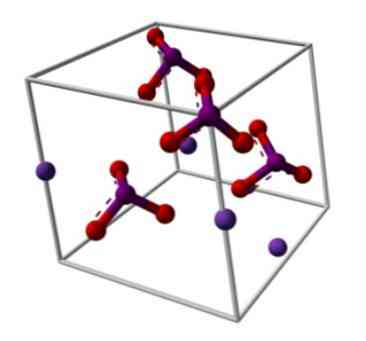
Chemická štruktúra jodičnanu draselného je znázornená na hornom obrázku. IO anión3- je reprezentovaný "statívom" červených a fialových guľôčok, zatiaľ čo K ióny+ sú reprezentované fialovými guľami.
Čo však znamenajú tieto statívy? Správne geometrické tvary týchto aniónov sú vlastne trigonálne pyramídy, v ktorých oxygény tvoria trojuholníkovú základňu, a nezdieľaný pár elektrónov v jódových bodoch smerom nahor, zaberajúci priestor a nútiaci spojenie IO dole a dva odkazy I = O.
Táto molekulová geometria zodpovedá sp hybridizácii3 centrálneho atómu jódu; avšak iná perspektíva naznačuje, že jeden z atómov kyslíka tvorí väzby s "d" orbitálmi jódu, čo je v skutočnosti sp hybridizácia3d2 (jód môže mať svoje "d" orbitály rozširujúce svoju valenčnú škrupinu).
Kryštály tejto soli môžu prejsť prechodmi štrukturálnej fázy (iné usporiadania ako monoklinické) v dôsledku rôznych fyzikálnych podmienok, ktoré ich vystavujú.
Použitie a aplikácie jodičnanu draselného
Terapeutické použitie
Jodičnan draselný sa zvyčajne používa na prevenciu akumulácie rádioaktivity v štítnej žľaze vo forme 131I, keď sa tento izotop používa na stanovenie príjmu jódu štítnou žľazou ako zložky funkcie štítnej žľazy.
Podobne sa jodičnan draselný používa ako lokálne antiseptikum (0,5%) pri slizničných infekciách.
Použitie v priemysle
Pridáva sa do krmiva hospodárskych zvierat ako doplnok jódu. Preto sa v priemysle používa jodičnan draselný na zlepšenie kvality múky.
Analytické použitie
V analytickej chémii sa vďaka svojej stabilite používa ako primárny štandard pri štandardizácii štandardných roztokov tiosíranu sodného (Na).2S2O3), aby sa stanovili koncentrácie jódu vo vzorkách.
To znamená, že množstvá jódu môžu byť známe pomocou objemových techník (titrácie). V tejto reakcii jodičnan draselný rýchlo oxiduje jodidové ióny I-, nasledujúcou chemickou rovnicou:
IO3- + 5I- + 6H+ => 3I2 + 3H2O
Jód, ja2, je pomenovaný roztokom Na2S2O3 normalizáciu.
Použitie v laserovej technológii
Štúdie preukázali a potvrdili zaujímavé piezoelektrické, pyroelektrické, elektrooptické, feroelektrické vlastnosti a v nelineárnej optike kryštálov KIO3. Výsledkom je veľký potenciál v oblasti elektroniky a technológie laserov pre materiály vyrobené s touto zlúčeninou.
Zdravotné riziká jodičnanu draselného
Vo vysokých dávkach môže spôsobiť podráždenie ústnej sliznice, kože, očí a dýchacích ciest.
Experimenty toxicity jodičnanu draselného u zvierat umožnili pozorovať, že u psov nalačno, pri dávkach 0,2-0,25 g / kg telesnej hmotnosti, podávaných orálne, zlúčenina spôsobuje zvracanie..
Ak sa tieto zvracania vyhnú, spôsobí zhoršenie situácie u zvierat, pretože pred smrťou indukuje anorexiu a prostráciu. Jeho pitvy umožnili pozorovať nekrotické lézie v pečeni, obličkách a črevnej sliznici.
Vzhľadom na svoju oxidačnú silu predstavuje nebezpečenstvo požiaru pri kontakte s horľavými materiálmi.
referencie
- Deň, R., & Underwood, A. Kvantitatívna analytická chémia (piate vydanie). PEARSON Prentice Hall, p-364.
- Muth, D. (2008). Lasery [obrázok]. Zdroj: flickr.com
- ChemicalBook. (2017). Jodičnan draselný. Zdroj: marec 25, 2018, z ChemicalBook: chemicalbook.com
- PubChem. (2018). Jodičnan draselný. Získané 25. marca 2018, z PubChem: pubchem.ncbi.nlm.nih.gov
- Merck. (2018). Jodičnan draselný. Získané 25. marca 2018 od spoločnosti Merck:
- merckmillipore.com
- Wikipedia. (2017). Jodičnan draselný. Získané dňa 25. marca 2018, z Wikipédie: sk.wikipedia.org
- M M Abdel Kader a kol. (2013). Mechanizmus prenosu náboja a fázové prechody s nízkou teplotou v KIO3. J. Phys., Conf., Ser 423 012036


