Proces exotermnej reakcie, typy a príklady
exotermická reakcia je typ chemickej reakcie, pri ktorej dochádza k prenosu energie, najmä vo forme uvoľňovania tepla alebo svetla. Názov pochádza z gréckej predpony exo, čo znamená „v zahraničí“; a termín "tepelný", ktorý označuje teplo alebo teplotu.
V tomto zmysle môžu exotermické reakcie prenášať iné druhy energie do prostredia, kde sa vytvárajú, ako sú výbuchy a ich spôsob prenosu kinetickej a zvukovej energie, keď sa látky, ktoré sú v plynnej fáze pri vysokých teplotách, rozširujú. násilným spôsobom.
V prípade použitia batérií sa tiež vykonáva exotermická reakcia, v tomto prípade sa elektrická energia prepravuje.
index
- 1 Proces
- 2 Typy
- 2.1 Spaľovacie reakcie
- 2.2 Neutralizačné reakcie
- 2.3 Oxidačné reakcie
- 2.4 Termitová reakcia
- 2.5 Reakčná polymerizácia
- 2.6 Jadrová štiepna reakcia
- 2.7 Iné reakcie
- 3 Príklady
- 4 Odkazy
proces
Predtým bolo spomenuté, že keď nastane exotermická reakcia, dochádza k uvoľneniu energie, ktorá môže byť ľahšie vizualizovaná v nasledujúcej rovnici:
Reagenty → Produkt (y) + energia
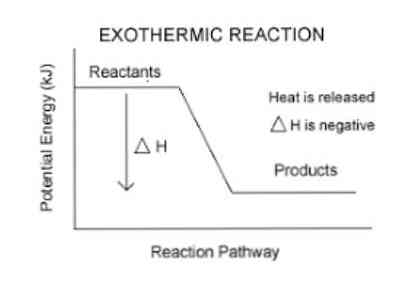
Takže na kvantifikáciu energie absorbovanej alebo uvoľnenej systémom sa používa termodynamický parameter nazývaný entalpia (označený ako "H"). Ak v systéme (v tomto prípade chemická reakcia) dochádza k uvoľneniu energie do okolia, potom zmena entalpie (vyjadrená ako ΔH) bude mať zápornú hodnotu.
V opačnom prípade, ak je variácia tohto opatrenia pozitívna, odráža absorpciu tepla z okolia. Veľkosť entalpickej variácie systému je tiež vyjadrením množstva energie, ktorá sa prenáša do prostredia alebo z neho..
Čím väčšia je hodnota AH, tým väčšie je uvoľňovanie energie zo systému do okolitého média.
Je to preto, že v týchto reakciách je čistá energia, ktorá sa uvoľní, keď sa vytvoria nové prepojenia, väčšia ako čistá energia použitá pri fragmentácii prepojení..
Z vyššie uvedeného je možné vyvodiť, že tento druh reakcií je veľmi bežný, pretože produkty reakcie majú množstvo energie uložené vo väzbách, ktoré je väčšie ako množstvo obsiahnuté v reaktantoch..
typ
Existujú rôzne druhy exotermických reakcií v rôznych oblastiach chémie, či už v laboratóriu alebo v priemysle; niektoré sa uskutočňujú spontánne a iné vyžadujú špecifické podmienky alebo nejaký druh látky, ako je napríklad katalyzátor, ktorý sa má vyrobiť.
Najdôležitejšie typy exotermických reakcií sú nasledovné:
Reakcie spaľovania
Reakcie spaľovania sú reakcie redoxného typu, ktoré sa vyskytujú, keď jedna alebo viac látok reaguje s kyslíkom, čo všeobecne vedie k uvoľňovaniu svetla a tepelnej energie - čo je svetlo a teplo - keď sa vytvára plameň..
Neutralizačné reakcie
Neutralizačné reakcie sú charakterizované interakciou medzi kyslým druhom a alkalickou látkou (bázou) za vzniku soli a vody, ktoré vykazujú exotermickú povahu.
Oxidačné reakcie
Existuje mnoho reakcií tohto typu, ktoré vykazujú exotermické správanie, pretože oxidácia kyslíka spôsobuje uvoľňovanie veľkého množstva energie, ako je to pri oxidácii uhľovodíkov..
Termitová reakcia
Táto reakcia môže viesť k teplote približne 3000 ° C a vďaka vysokej afinite hliníkového prášku s veľkým počtom oxidov kovov sa používa pri zváraní ocele a železa..
Polymerizačná reakcia
Tento typ reakcie je taký, ktorý vzniká, keď určitý počet chemických druhov, ktoré sa nazývajú monoméry, reaguje, čo sú jednotky, ktoré v kombinácii sa opakujú v reťazcoch za vzniku makromolekulových štruktúr nazývaných polyméry..
Reakcia jadrového štiepenia
Tento proces sa vzťahuje na rozdelenie jadra atómu považovaného za ťažký - to znamená, že s hmotnostným číslom (A) väčším ako 200 - produkuje fragmenty alebo jadrá menšej veľkosti s medziľahlou hmotnosťou..
V tejto reakcii, keď sa tvorí jeden alebo viac neutrónov, sa uvoľňuje veľké množstvo energie, pretože jadro s vyššou hmotnosťou má nižšiu stabilitu ako jeho produkty..
Iné reakcie
Existujú aj iné exotermické reakcie, ktoré sú veľmi dôležité, ako napríklad dehydratácia niektorých sacharidov pri reakcii s kyselinou sírovou, absorpcia vody, ktorá má hydroxid sodný vystavený na voľnom priestranstve alebo oxidácia kovových druhov pri mnohých koróznych reakciách..
Príklady
Nižšie sú uvedené príklady exotermických reakcií, ktoré spôsobujú zmenu entalpie, ktorá má zápornú hodnotu v dôsledku skutočnosti, že uvoľňujú energiu, ako je uvedené vyššie..
Napríklad spaľovanie propánu je spontánna exotermická reakcia:
C3H8(g) + 5O2(g) → 3CO2(g) + 4H2O (l)
Ďalším prípadom exotermického správania je neutralizačná reakcia medzi uhličitanom sodným a kyselinou chlorovodíkovou:
hydrogénuhličitan sodný3(ac) + HCl (ac) → NaCl (ac) + H2O (l) + CO2(G)
Predložená je tiež oxidácia etanolu na kyselinu octovú použitú v dychových analyzátoroch, ktorých úplná reakcia je znázornená v nasledujúcej rovnici:
3CH3CH2OH + 2K2Cr2O7 + 8H2SW4 → CH3COOH + 2Cr (SO4)3 + 2K2SW4 + 11H2O
Ďalšou triedou exotermickej reakcie je takzvaná termitová reakcia, pri ktorej sa hliník kombinuje s oxidom kovu, ako je uvedené nižšie:
2Al (s) + Viera2O3(s) → Al2O3(s) + Fe (l)
Okrem vyššie uvedených príkladov existuje široká škála reakcií, ktoré sa tiež považujú za exotermické, ako je rozklad určitých organických odpadových látok na kompostovanie..
Zdôrazňuje tiež oxidáciu luciferínového pigmentu pôsobením enzýmu luciferázy na produkciu bioluminiscencie charakteristickej pre svetlušky a dokonca aj dýchanie, medzi mnohými ďalšími reakciami..
referencie
- Wikipedia. (N. D.). Exotermická reakcia. Zdroj: es.wikipedia.org
- BBC. (N. D.). Energetické zmeny a reverzibilné reakcie. Získané z bbc.co.uk
- Chang, R. (2007). Chémia, deviate vydanie. (McGraw-Hill).
- Walker, D. (2007). Chemické reakcie. Zdroj: books.google.co.ve
- Saunders, N. (2007). Skúmanie chemických reakcií. Zdroj: books.google.co.ve


