Joseph Thomson Životopis a príspevky k vede a chémii
Joseph John Thomson Bol prominentným chemikom pre rôzne príspevky, ako napríklad objav elektrónu, jeho atómový model, objav izotopov alebo experiment katódového lúča.
Narodil sa v Cheetam Hill, okrese Manchester, Anglicko, 18. decembra 1856. Tiež známy ako "J.J." Thomson, študoval inžinierstvo na Owens College, teraz súčasť University of Manchester, a neskôr, matematika na Cambridge.

V roku 1890 sa J. J. Thomson oženil s Rose Elizabeth Paget, dcérou lekára Sir Edward George Paget, s ktorým som mal dve deti: dievča menom Joan Paget Thomson a chlapca George Paget Thomson.
Ten by sa stal slávnym vedcom, ktorý získal v roku 1937 Nobelovu cenu za fyziku za svoju prácu s elektrónmi.
Od mladého veku Thomson zameral svoje štúdie na štruktúru atómov, a tak objavil existenciu elektrónov a izotopov, medzi mnoho ďalších príspevkov.
V roku 1906, Thomson dostal Nobelovu cenu za fyziku, "v uznaní veľké zásluhy jeho teoretické a experimentálny výskum o vedení elektriny cez plyny", medzi mnoho ďalších ocenení za jeho prácu. (1)
V roku 1908 bol rytierom britskej koruny a pôsobil ako čestný profesor fyziky na Cambridge a na Royal Institute v Londýne..
Zomrel 30. augusta 1940, v 83, v meste Cambridge, Spojené kráľovstvo. Fyzik bol pochovaný v opátstve Westminster, neďaleko hrobky Sira Isaaca Newtona. (2)
index
- 1 Hlavné príspevky spoločnosti Thomson k vede
- 1.1 Objav elektrónu
- 1.2 Thomsonov atómový model
- 1.3 Separácia atómov
- 1.4 Objav izotopov
- 1.5 Experimenty s katódovými lúčmi
- 1.6 Hmotnostný spektrometer
- 2 Odkaz Thomsona
- 3 Najlepšie práce
- 4 Odkazy
Hlavné príspevky spoločnosti Thomson k vede
Objav elektrónu
V roku 1897 J.J. Thomson objavil novú časticu ľahšiu ako vodík, ktorý bol pokrstený "elektrón".
Vodík bol považovaný za jednotku merania atómovej hmotnosti. Do tej doby bol atóm najmenším rozdelením hmoty.
V tomto zmysle bol Thomson prvý, kto objavil negatívne nabité korpuskulárne subatomárne častice.
Atómový model Thomsona
Thomsonov atómový model bola štruktúra, ktorú anglický fyzik pripisoval atómom. Pre vedca boli atómy sférou pozitívneho náboja.
Tam boli negatívne nabité elektróny, rovnomerne rozložené na tomto pozitívne nabitom oblaku, vložené a neutralizovali pozitívny náboj hmoty atómu..
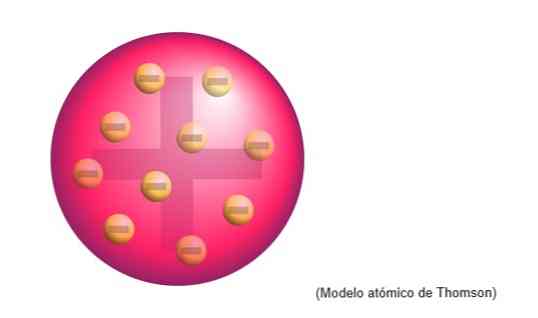
Tento nový model nahrádza model vypracovaný Daltonom a neskôr ho vyvráti Rutherford, žiak Thomsona v Cavendish Laboratories, Cambridge.
Separácia atómov
Thomson použil pozitívne alebo anodické lúče na oddelenie atómov rôznej hmotnosti. Táto metóda mu umožnila vypočítať elektrinu prenášanú každým atómom a počet molekúl na centimeter kubický.
Fyzik tým, že dokáže rozdeliť atómy rôznej hmotnosti a náboja, objavil existenciu izotopov. Aj týmto spôsobom, so štúdiom pozitívnych lúčov, urobil veľký pokrok smerom k hmotnostnej spektrometrii.
Objav izotopov
J.J. Thomson zistil, že neónové ióny majú rôzne hmotnosti, to znamená rôzne atómové hmotnosti. Takto Thomson ukázal, že neón má dva podtypy izotopov, neón-20 a neón-22..
Izotopy, študované dodnes, sú atómy toho istého prvku, ale ich jadrá majú rôzne hmotnostné čísla, pretože sú zložené z rôznych množstiev neutrónov v ich strede.
Experimenty s katódovými lúčmi
Katódové lúče sú elektrónové prúdy vo vákuových trubiciach, tj sklenené trubice s dvoma elektródami, jedna pozitívna a jedna negatívna.
Keď sa záporná elektróda, alebo tiež katóda, zahrieva, vyžaruje žiarenie, ktoré je nasmerované na kladnú elektródu alebo anódu v priamke, ak v tejto dráhe nie je prítomné žiadne magnetické pole..
Ak sú steny trubicového skla pokryté fluorescenčným materiálom, náraz katód proti tejto vrstve vytvára projekciu svetla.
Thomson študoval správanie katódových lúčov a dospel k záverom, že lúče sa šíria v priamke.
Tiež, že tieto lúče by sa mohli odchýliť od ich trajektórie prítomnosťou magnetu, teda magnetického poľa. Okrem toho by lúče mohli pohybovať lopatkami so silou hmoty elektrónov, ktoré cirkulujú, čo dokazuje, že elektróny mali hmotnosť.
J.J. Thomson experimentoval s tým, že mení plyn v katódovej trubici, ale správanie elektrónov sa nemení. Tiež katódové lúče ohriali predmety, ktoré sa dostali medzi elektródy.
Na záver, Thomson ukázal, že katódové lúče majú svetelné, mechanické, chemické a tepelné účinky.
Katódové trubice a ich svetelné vlastnosti boli transcendentné pre neskorší vynález televíznej trubice (CTR) a videokamier..
Hmotnostný spektrometer
J.J. Thomson vytvoril prvý prístup hmotnostný spektrometer. Tento nástroj umožnil vedcovi študovať pomer hmotnosť / náboj katódových trubíc a merať, koľko sú odklonené vplyvom magnetického poľa a množstva energie, ktorú prenášajú..
S týmto výskumom dospel k záveru, že katódové lúče boli zložené zo záporne nabitých teliesok, ktoré sú vo vnútri atómov, čím sa postuluje deliteľnosť atómu a dochádza k vzniku postavy elektrónu..
Podobne pokroky v hmotnostnej spektrometrii pokračovali až do súčasnosti, vyvíjajúc sa v rôznych metódach na separáciu elektrónov od atómov.
Okrem toho Thomson navrhol ako prvý prvý vlnovod Tento experiment spočíval v šírení elektromagnetických vĺn v kontrolovanej valcovej dutine, ktorá bola prvýkrát vykonaná v roku 1897 Lordom Rayleighom, ďalšou Nobelovou cenou za fyziku..
V budúcnosti budú vlnovody široko používané, dokonca aj dnes s prenosom dát a optickými vláknami.
Odkaz Thomsona
Thomson (Th) bol založený ako jednotka merania hmotnostného zaťaženia v hmotnostnej spektrometrii, ktorú navrhli chemici Cooks a Rockwood na počesť Thomsona.
Táto technika umožňuje určiť distribúciu molekúl látky podľa jej hmotnosti a rozpoznať ju, ktoré sú prítomné vo vzorke hmoty..
Thomsonov vzorec (Th):

Najlepšie práce
- Odpad elektriny plynom, vedenie elektriny plynom (1900).
- Korpuskulárna teória hmoty, elektrón v chémii a spomienkach a odrazoch (1907).
- Za elektrónom (1928).
referencie
- Nobel Media AB (2014). J. Thomson - Životopis. Nobelprize.org. nobelprize.org.
- Thomson, Joseph J., Vedenie elektriny cez plyny. Cambridge, University Press, 1903.
- Menchaca Rocha, Arturo. Diskrétne kúzlo elementárnych častíc.
- Christen, Hans Rudolf, Základy všeobecnej a anorganickej chémie, zväzok 1. Barcelona, Španielsko. Ediciones Reverté S.A., 1986.
- Arzani, Aurora Cortina, Všeobecná elementárna chémia. Mexiko, Editorial Porrúa, 1967.
- R. G. Cooks, A. L. Rockwood. Rapid Commun. Hmotnostné spektrum. 5, 93 (1991).


