História kalorimetra, časti, typy a ich vlastnosti
kalorimeter je zariadenie, ktoré sa používa na meranie zmeny teploty množstva látky (zvyčajne vody) známeho špecifického tepla. Táto zmena teploty je spôsobená teplom absorbovaným alebo uvoľneným v procese, ktorý sa študuje; chemická, ak ide o reakciu, alebo fyzikálna, ak pozostáva zo zmeny fázy alebo stavu.
V laboratóriu je najjednoduchším kalorimetrom, ktorý sa nachádza v šálke kávy. Používa sa na meranie tepla absorbovaného alebo uvoľneného pri reakcii pri konštantnom tlaku vo vodnom roztoku. Reakcie sa volia tak, aby sa zabránilo zásahu činidiel alebo plynných produktov.
 Pri exotermickej reakcii sa množstvo tepla, ktoré sa uvoľní, môže vypočítať zo zvýšenia teploty kalorimetra a vodného roztoku:
Pri exotermickej reakcii sa množstvo tepla, ktoré sa uvoľní, môže vypočítať zo zvýšenia teploty kalorimetra a vodného roztoku:
Množstvo tepla, ktoré sa uvoľňuje v reakcii = množstvo tepla absorbovaného kalorimetrom + množstvo tepla absorbovaného roztokom \ t
Množstvo tepla absorbovaného kalorimetrom sa nazýva kalorimetrický kalorický výkon. Toto sa stanoví privedením známeho množstva tepla do kalorimetra daným množstvom vody. Potom sa meria zvýšenie teploty kalorimetra a roztok, ktorý obsahuje.
S týmito údajmi a použitím špecifického tepla vody (4,18 J / g.ºC) je možné vypočítať kalorickú kapacitu kalorimetra. Táto kapacita sa tiež nazýva kalorimetrová konštanta.
Na druhej strane teplo získané vodným roztokom sa rovná m · ce · At. Vo vzorci m = hmotnosť vody, ce = špecifické teplo vody a Δt = zmena teploty. Keď toto všetko poznáme, je možné vypočítať množstvo tepla uvoľneného exotermickou reakciou.
index
- 1 História kalorimetra
- 2 Diely
- 3 Typy a ich vlastnosti
- 3.1 Šálka kávy
- 3.2 Kalorimetrické čerpadlo
- 3.3 Adiabatický kalorimeter
- 3.4 Isoperibolický kalorimeter
- 3.5 Prietokový kalorimeter
- 3.6 Kalorimeter pre diferenciálnu skenovaciu kalorimetriu
- 4 Aplikácie
- 4.1 Vo fyzikálno-chemickej oblasti
- 4.2 V biologických systémoch
- 4.3 Kalorimeter kyslíkovej pumpy a kalorický výkon
- 5 Referencie
História kalorimetra
V roku 1780, A. L. Lavoisier, francúzsky chemik, považovaný za jedného z otcov chémie, používal morča na meranie produkcie tepla jeho dýchaním.
Ako? Použitie zariadenia podobného kalorimetra. Teplo produkované morčaťom bolo dokázané roztavením snehu, ktorý obklopoval zariadenie.
Výskumníci A. L Lavoisier (1743-1794) a P. S. Laplace (1749-1827) navrhli kalorimeter, ktorý sa použil na meranie špecifického tepla tela metódou tavenia ľadu.
Kalorimeter pozostával z pocínovanej cylindrickej kadičky, lakovanej, držanej statívom a vnútorne zakončenej lievikom. Vo vnútri sa umiestnilo ďalšie sklo, podobné predchádzajúcemu, s trubicou, ktorá prešla vonkajšou komorou a ktorá bola vybavená kľúčom. V druhej skle bola mriežka.
V tejto mriežke bola umiestnená byt alebo predmet, ktorého špecifické teplo bolo žiaduce určiť. Ľad bol umiestnený vnútri sústredných nádob, presne ako v koši.
Teplo produkované telom bolo absorbované ľadom, čo spôsobilo jeho fúziu. Kvapalný vodný produkt roztavenia ľadu sa zozbieral, čím sa otvoril kľúč vnútorného skla.
A nakoniec, zváženie vody, hmotnosť roztaveného ľadu bola známa.
diely
Najčastejšie používaným kalorimetrom v laboratóriách vyučujúcich chémiu je tzv. Kalorimeter kávového pohára. Tento kalorimeter sa skladá z kadičky alebo namiesto toho nádoby z anime materiálu, ktorá má určité izolačné vlastnosti. Vo vnútri nádoby je vodný roztok umiestnený s telom, ktoré produkuje alebo absorbuje teplo.
V hornej časti kontajnera je umiestnený kryt izolačného materiálu s dvoma otvormi. V jednom je teplomer zavedený na meranie teplotných zmien a v druhom je miešadlo, výhodne zo skleneného materiálu, ktorý plní funkciu pohybu obsahu vodného roztoku..
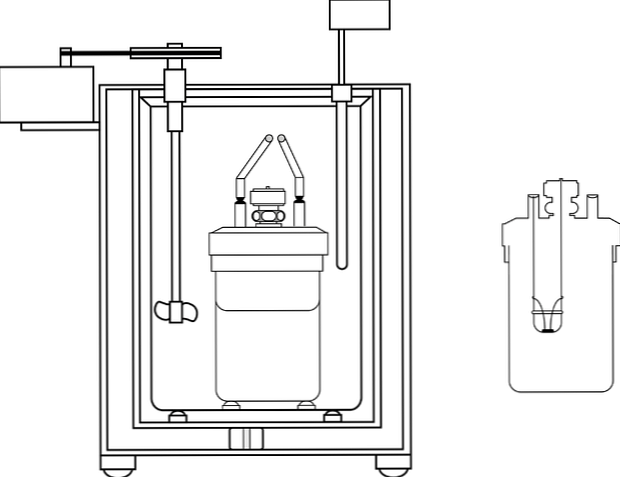
Obrázok zobrazuje časti kalorimetrického čerpadla; možno však pozorovať, že má teplomer a miešadlo, spoločné prvky v niekoľkých kalorimetroch.
Druhy a ich vlastnosti
Šálka kávy
Je to ten, ktorý sa používa na stanovenie tepla uvoľneného exotermickou reakciou a tepla absorbovaného v endotermickej reakcii..
Okrem toho sa môže použiť pri určovaní špecifického tepla tela; to znamená množstvo tepla, ktoré musí gram látky absorbovať, aby sa zvýšila jeho teplota o jeden stupeň Celzia. .
Kalorimetrické čerpadlo
Je to zariadenie, v ktorom sa meria množstvo tepla, ktoré sa uvoľňuje alebo absorbuje v reakcii, ku ktorej dochádza pri konštantnom objeme.
Reakcia prebieha v silnej oceľovej nádobe (čerpadle), ktorá je ponorená do veľkého objemu vody. Tým sú zmeny teploty vody malé. Preto sa predpokladá, že zmeny spojené s reakciou sa merajú pri konštantnej teplote a objeme.
Z vyššie uvedeného vyplýva, že sa nevykonáva žiadna práca, keď sa reakcia uskutočňuje v kalorimetrickom čerpadle.
Reakcia začína dodávkou elektriny cez káble pripojené k čerpadlu.
Adiabatický kalorimeter
Vyznačuje sa tým, že má izolačnú štruktúru nazývanú štít. Štít je umiestnený okolo článku, kde dochádza k tepelným a teplotným zmenám. Je tiež spojený s elektronickým systémom, ktorý udržuje svoju teplotu veľmi blízku teplote článku, aby sa zabránilo prenosu tepla.
V adiabatickom kalorimetri je teplotný rozdiel medzi kalorimetrom a jeho okolím minimalizovaný; ako aj minimalizovanie koeficientu prenosu tepla a času výmeny tepla.
Jej časti tvoria:
-Bunka (alebo nádoba) je integrovaná do izolačného systému, ktorým sa snaží zabrániť tepelným stratám.
-Teplomer na meranie teplotných zmien.
-Ohrievač, pripojený k ovládateľnému zdroju elektrického napätia.
-A štít, už spomínaný.
V tomto type kalorimetra je možné určiť vlastnosti ako entropia, Debyova teplota a hustota elektronického stavu.
Izoperibolický kalorimeter
Je to zariadenie, v ktorom sú reakčná bunka a čerpadlo ponorené do štruktúry nazývanej plášť. V tomto prípade sa takzvaný plášť skladá z vody, udržiavanej na konštantnej teplote.
Teplota článku a čerpadlo sa zvyšujú, keď sa počas spaľovacieho procesu uvoľňuje teplo; ale teplota vodného plášťa sa udržiava na pevnej teplote.
Mikroprocesor riadi teplotu článku a plášťa, pričom vykonáva potrebné korekcie úniku tepla, ktoré vyplývajú z rozdielov medzi týmito dvoma teplotami..
Tieto korekcie sa aplikujú nepretržite as konečnou korekciou na základe meraní pred a po teste.
Prietokový kalorimeter
Vyvinutý Caliendar má zariadenie na pohyb plynu v kontajneri konštantnou rýchlosťou. Pri pridávaní tepla sa meria zvýšenie teploty v kvapaline.
Prietokový kalorimeter sa vyznačuje:
- Presné meranie konštantného prietoku.
- Presné meranie množstva tepla privádzaného do kvapaliny cez ohrievač.
- Presné meranie zvýšenia teploty v plyne spôsobenej prívodom energie
- Konštrukcia na meranie kapacity plynu pod tlakom.
Kalorimeter pre diferenciálnu skenovaciu kalorimetriu
Vyznačuje sa dvoma nádobami: v jednej sa umiestni skúmaná vzorka, zatiaľ čo druhá sa ponechá prázdna alebo sa použije referenčný materiál..
Obe nádoby sa ohrievajú konštantnou rýchlosťou energie pomocou dvoch nezávislých ohrievačov. Keď začne ohrievanie oboch nádob, počítač bude zaznamenávať rozdiel tepelného toku ohrievačov voči teplote, čím bude schopný určiť tok tepla.
Okrem toho môže byť určená zmena teploty ako funkcie času; a nakoniec kalorickú kapacitu.
aplikácie
Vo fyziochémii
-Základné kalorimetre, typ kávového šálky, umožňujú merať množstvo tepla, ktoré telo uvoľňuje alebo absorbuje. Môžu určiť, či je reakcia exotermická alebo endotermická. Okrem toho je možné určiť špecifické teplo tela.
-Pomocou adiabatického kalorimetra bolo možné určiť entropiu chemického procesu a elektronickú hustotu stavu.
V biologických systémoch
-Mikrokalorimetre sa používajú na štúdium biologických systémov, ktoré zahŕňajú interakcie medzi molekulami, ako aj zmeny molekulárnych konformácií, ktoré sa vyskytujú; napríklad pri rozvinutí molekuly. Čiara obsahuje diferenciálnu aj izotermickú titráciu.
-Mikrokalimeter sa používa pri vývoji liekov malých molekúl, bioterapeutík a vakcín.
Kalorimeter a kalorický výkon kyslíkového čerpadla
Spaľovanie mnohých látok sa uskutočňuje v kalorimetri kyslíkovej pumpy a je možné určiť jeho kalorickú energiu. Medzi látkami študovanými použitím tohto kalorimetra patria: uhlie a koks; jedlé oleje, ťažké aj ľahké; benzín a všetky motorové palivá.
Ako aj druhy palív pre letecké reaktory; Odpad z paliva a likvidácia odpadu; potravinové výrobky a doplnky pre ľudskú výživu; krmoviny a potravinové doplnky; stavebné materiály; a palív na pohonné hmoty.
Podobne kalorická energia bola stanovená kalorimetricky v termodynamických štúdiách horľavých materiálov; v štúdiu energetickej rovnováhy v ekológii; vo výbušninách a tepelných práškoch a vo výučbe základných termodynamických metód.
referencie
- Whitten, Davis, Peck & Stanley. Chémia. (8. vydanie). CENGAGE Učenie.
- González J., Cortés L. & Sánchez A. (s.f.). Adiabatická kalorimetria a jej aplikácie. Získané z: cenam.mx
- Wikipedia. (2018). Kalorimeter. Zdroj: en.wikipedia.org
- Helmenstine, Anne Marie, Ph.D. (22. júna 2018). Definícia kalorimetra v chémii. Zdroj: thinkco.com
- Gillespie, Claire. (11. apríl 2018). Ako funguje kalorimeter? Sciencing. Zdroj: sciencing.com


