Štruktúra, vlastnosti, syntéza, použitie a riziká etyl acetátu
etylacetát alebo etyletanoát (IUPAC názov) je organická zlúčenina, ktorej chemický vzorec je CH3COOC2H5. Skladá sa z esteru, kde alkoholová zložka pochádza z etanolu, zatiaľ čo jeho zložka karboxylovej kyseliny pochádza z kyseliny octovej.
Je to kvapalina za normálnych podmienok teploty a tlaku, ktorá predstavuje príjemnú vôňu ovocia. Táto vlastnosť vstupuje dokonale do súladu s tým, čo sa očakáva od esteru; čo je v skutočnosti chemická povaha etylacetátu. Z tohto dôvodu nájde uplatnenie v potravinárskych výrobkoch a alkoholických nápojoch.
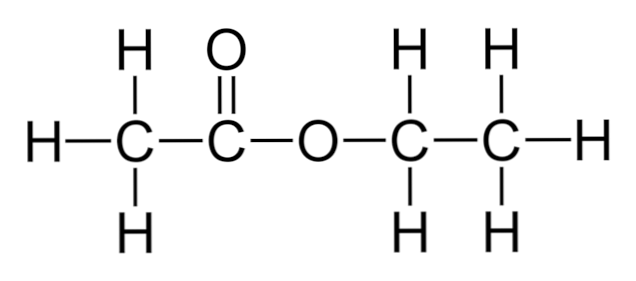
Na hornom obrázku je znázornená štruktúra štruktúry etylacetátu. Všimnite si ľavú zložku karboxylovej kyseliny a vpravo alkoholovú zložku. Zo štrukturálneho hľadiska sa dá očakávať, že sa táto zlúčenina správa ako hybrid medzi octom a alkoholom; vykazuje však svoje vlastné vlastnosti.
Toto je miesto, kde takéto hybridy nazývané estery vystupujú ako odlišné. Etylacetát nemôže reagovať ako kyselina, ani nemôže dehydratovať v neprítomnosti OH skupiny. Namiesto toho prechádza zásaditou hydrolýzou v prítomnosti silnej bázy, ako je hydroxid sodný, NaOH.
Táto hydrolytická reakcia sa používa vo vyučovacích laboratóriách na chemické kinetické experimenty; kde reakcia je navyše v druhom poradí. Keď dôjde k hydrolýze, prakticky etyletanoát sa vracia do svojich pôvodných zložiek: kyselina (deprotonovaná NaOH) a alkohol.
Vo svojej konštrukčnej štruktúre sa pozoruje, že atómy vodíka prevládajú nad atómami kyslíka. To ovplyvňuje ich schopnosť interakcie s nepolárnymi druhmi, ako sú tuky. Používa sa tiež na rozpúšťanie zlúčenín, ako sú živice, farbivá a všeobecne organické tuhé látky.
Dlhodobá expozícia tejto kvapaline má napriek príjemnej aróme negatívny vplyv (ako takmer všetky chemické zlúčeniny) v tele.
index
- 1 Štruktúra etylacetátu
- 1.1 Absencia atómov donorov vodíka
- 2 Fyzikálne a chemické vlastnosti
- 2.1 Názvy
- 2.2 Molekulový vzorec
- 2.3 Molekulová hmotnosť
- 2.4 Fyzický popis
- 2,5 Farba
- 2.6 Vôňa
- 2.7 Chuť
- 2.8 Prahová hodnota zápachu
- 2.9 Teplota varu
- 2.10 Teplota topenia
- 2.11 Rozpustnosť vo vode
- 2.12 Rozpustnosť v organických rozpúšťadlách
- 2.13 Hustota
- 2.14 Hustota pár
- 2.15 Stabilita
- 2.16 Tlak pár
- 2.17 Viskozita
- 2.18 Teplo spaľovania
- 2.19 Teplo na odparovanie
- 2.20 Povrchové napätie
- 2.21 Index lomu
- 2.22 Skladovacia teplota
- 2,23 pKa
- 3 Zhrnutie
- 3.1 Fisherova reakcia
- 3.2 Tishchenkova reakcia
- 3.3 Iné metódy
- 4 Použitie
- 4.1 Rozpúšťadlo
- 4.2 Umelé príchute
- 4.3 Analytics
- 4.4 Organická syntéza
- 4.5 Chromatografia
- 4.6 Entomológia
- 5 Riziká
- 6 Referencie
Štruktúra etylacetátu
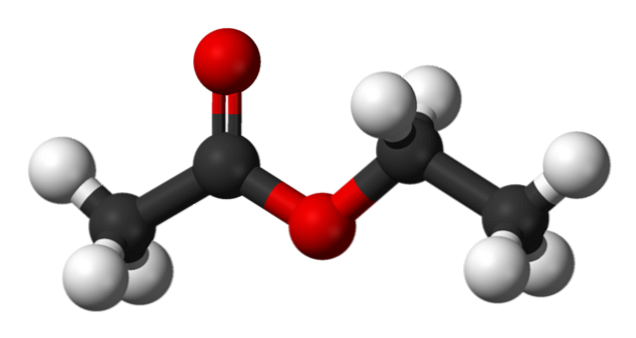
V hornom obrázku je znázornená štruktúra etylacetátu s modelom guľôčok a tyčiniek. V tomto modeli sú zvýraznené atómy kyslíka s červenými guľami; vľavo je frakcia odvodená od kyseliny a vpravo je frakcia odvodená od alkoholu (alkoxyskupina, -OR).
Karbonylová skupina je ocenená väzbou C = 0 (dvojité stĺpce). Štruktúra okolo tejto skupiny a priľahlého kyslíka je plochá, pretože dochádza k delokalizácii záťaže rezonanciou medzi oboma kyslíkami; skutočnosť, ktorá vysvetľuje relatívne nízku kyslosť a-vodíkov (skupiny -CH skupiny3, spojené s C = O).
Molekula rotáciou dvoch svojich väzieb priamo uprednostňuje interakciu s inými molekulami. Prítomnosť dvoch atómov kyslíka a asymetria v štruktúre mu dávajú permanentný dipólový moment; ktoré sú zase zodpovedné za ich dipólovo-dipólové interakcie.
Napríklad elektronická hustota je väčšia v blízkosti dvoch atómov kyslíka, pričom sa značne znižuje v skupine -CH3, a postupne v skupine OCH2CH3.
Vďaka týmto interakciám tvoria molekuly etylacetátu za normálnych podmienok kvapalinu, ktorá má značne vysokú teplotu varu (77 ° C)..
Absencia donorových atómov vodíkových väzieb
Ak sa pozriete pozorne na štruktúru, všimnete si neprítomnosť atómu schopného darovať vodíkový most. Atómy kyslíka sú však také akceptory a etylacetát je veľmi rozpustný vo vode a v značnej miere interaguje s polárnymi zlúčeninami a donormi vodíkových väzieb (ako sú cukry)..
To tiež umožňuje vynikajúcu interakciu s etanolom; preto jej prítomnosť v alkoholických nápojoch nie je prekvapujúca.
Na druhej strane jej alkoxylová skupina umožňuje interakciu s určitými nepolárnymi zlúčeninami, ako je chloroform, CH3cl.
Fyzikálne a chemické vlastnosti
mená
-Etylacetát
-Etyletanoát
-Ester kyseliny octovej
-Acetoxietano
Molekulový vzorec
C4H8O2 alebo CH3COOC2H5
Molekulová hmotnosť
88,106 g / mol.
Fyzický popis
Číra bezfarebná kvapalina.
farba
Bezfarebná kvapalina.
vône
Charakteristické pre étery, podobné vôni ananásu.
príchuť
Príjemný pri riedení, dodáva ovocnej chuti do piva.
Prahová hodnota zápachu
3,9 ppm. 0,0196 mg / m3 (nízky zápach); 665 mg / m3 (vysoký zápach).
Detekovateľný zápach pri 7 - 50 ppm (priemer = 8 ppm).
Teplota varu
171 ° F až 760 mmHg (77,1 ° C).
Teplota topenia
--83,8 ° C (-83,8 ° C).
Rozpustnosť vo vode
80 g / l.
Rozpustnosť v organických rozpúšťadlách
Miešateľný s etanolom a etyléterom. Veľmi rozpustný v acetóne a benzéne. Miešateľné aj s chloroformom, pevnými a prchavými olejmi a tiež s okysličenými a chlórovanými rozpúšťadlami.
hustota
0,9003 g / cm3.
Hustota pár
3,04 (v pomere vzduchu: 1).
stabilita
Rozkladá sa pomaly vlhkosťou; nekompatibilný s niekoľkými plastmi a silnými oxidačnými činidlami. Zmes s vodou môže byť výbušná.
Tlak pary
93,2 mmHg pri 25 ° C
viskozita
0,423 mPoise pri 25 ° C.
Teplo spaľovania
2,238,1 kJ / mol.
Odparovacie teplo
35,60 kJ / mol pri 25 ° C.
Povrchové napätie
24 dyn / cm pri 20 ° C.
Index lomu
1,373 pri 20 ° C / D.
Teplota skladovania
2 - 8 ° C.
pKa
16 - 18 pri 25 ° C.
syntéza
Fisherova reakcia
Etylacetát sa syntetizuje priemyselne pomocou Fisherovej reakcie, pri ktorej sa etanol esterifikuje kyselinou octovou. Reakcia sa uskutočňuje pri teplote miestnosti.
CH3CH2OH + CH3COOH <=> CH3Cooch2CH3 + H2O
Reakcia sa urýchľuje kyslou katalýzou. Rovnováha sa pohybuje doprava, to znamená smerom k produkcii etylacetátu, odstránením vody; podľa zákona hromadného konania.
Reakcia Tishchenka
Etylacetát sa tiež pripraví priemyselne s použitím reakcie Tishchenko, konjugáciou dvoch ekvivalentov acetaldehydu s použitím alkoxidu ako katalyzátora..
2 CH3CHO => CH3Cooch2CH3
Iné metódy
-Etylacetát sa syntetizuje ako ko-produkt pri oxidácii butánu na kyselinu octovú v reakcii uskutočňovanej pri teplote 175 ° C a tlaku 50 atm. Ako katalyzátor sa používajú kobalt a ióny chrómu.
-Etylacetát je vedľajším produktom etanolýzy polyvinylacetátu na polyvinylalkohol.
-Etylacetát sa tiež vyrába v priemysle dehydrogenáciou etanolu, pričom reakcia sa katalyzuje použitím medi pri zvýšenej teplote, ale nižšej ako 250 ° C..
aplikácie
rozpúšťadlo
Etylacetát sa používa ako rozpúšťadlo a riedidlo, ktoré sa používa na čistenie dosiek s obvodmi. Používa sa ako rozpúšťadlo pri výrobe modifikovaného chmeľového extraktu a pri odstraňovaní kofeínu kávy a čajových listov. Používa sa v atramentoch používaných na označovanie ovocia a zeleniny.
Etylacetát sa používa v textilnom priemysle ako čistiaci prostriedok. Používa sa pri kalibrácii teplomerov používaných pri separácii cukrov. V priemysle lakov sa používa ako rozpúšťadlo a riedidlo použitých materiálov.
Umelé arómy
Používa sa pri spracovaní ovocných príchutí; Napríklad: banán, hruška, broskyňa a ananás, ako aj hroznová aróma atď..
analytické
Používa sa na stanovenie bizmutu, bóru, zlata, molybdénu a platiny, ako aj táliového rozpúšťadla. Etylacetát má schopnosť extrahovať mnohé zlúčeniny a prvky prítomné vo vodnom roztoku, ako sú: fosfor, kobalt, volfrám a arzén..
Organické syntézy
Etylacetát sa používa v priemysle ako reduktor viskozity pre živice používané vo formuláciách fotorezistu. Používa sa pri výrobe acetamidu, acetylacetátu a metylheptanónu.
chromatografie
V laboratóriách sa ako mobilná fáza stĺpcovej chromatografie a ako extrakčné rozpúšťadlo použije etylacetát. Tým, že etylacetát má relatívne nízku teplotu varu, je ľahké odpariť, čo umožňuje koncentrovať rozpustené látky v rozpúšťadle.
entomológia
Etylacetát sa používa v entomológii na asfyxizáciu hmyzu umiestneného v nádobe, ktorá umožňuje jeho zber a štúdium. Pary etylacetátu zabíjajú hmyz bez toho, aby ho zničili a zabránili jeho vytvrdeniu, čo uľahčuje jeho montáž na zber.
riziká
-LD50 u potkanov indikuje nízku toxicitu. Môže však dráždiť pokožku, oči, pokožku, nos a hrdlo.
-Vystavenie vysokým úrovniam môže spôsobiť závraty a mdloby. Dlhodobá expozícia môže tiež ovplyvniť pečeň a obličky.
-Inhalácia etylacetátu v koncentrácii 20 000 - 43 000 ppm môže spôsobiť pľúcny edém a krvácanie.
-Pracovná expozičná hranica bola stanovená OSHA na 400 ppm vo vzduchu, v priemere počas 8-hodinovej pracovnej zmeny.
referencie
- Steven A. Hardinger. (2017). Ilustrovaný slovník organickej chémie: etylacetát (EtOAc). Zdroj: chem.ucla.edu
- Graham Solomons T.W., Craig B. Fryhle. (2011). Organická chémia. Amíny. (10th vydania.). Wiley Plus.
- Morrison, R. T. a Boyd, R. N. (1990). Organická chémia (5ta edition). Editorial Addison-Wesley Iberoamericana.
- Wikipedia. (2019). Etylacetát. Zdroj: en.wikipedia.org
- Bavlna S. (s.f.). Etylacetát. Zdroj: chm.bris.ac.uk
- PubChem. (2019). Etylacetát. Zdroj: pubchem.ncbi.nlm.nih.gov
- Newseed Chemical. (2018). Použitie a použitie etylacetátu. Zdroj: foodweeteners.com
- New Jersey Ministerstvo zdravotníctva Senior Services. (2002). Etylacetát. [PDF]. Zdroj: nj.gov


